Bevor der erste Weltkrieg begann, war bereits bekannt, dass Atome aus positiven Kernen und negativen Elektronen bestehen. Der neuseeländische Physiker Ernest Rutherford (1871-1937) hatte herausgefunden, dass der Beschuss einer Metallplatte mit Alpha-Teilchen zu einer charakteristischen Streuung der Strahlung führte. Die meisten α-Teilchen durchquerten die Platte ungehindert, einige wenige wurden jedoch in einem signifikanten Winkel abgelenkt. Daraus schloss Rutherford, dass das Atom aus einem sehr kleinen Atomkern mit positiver Ladung und einer Atomhülle (mit negativer Ladung) bestehen müsse (Rutherford 1911). Dieses Modell ist heute als Rutherford’sches Atommodell bekannt. Während die meisten α-Teilchen die Hülle ungehindert passieren, kommen einige wenige in die Nähe des Kerns und werden dort von der positiven Ladung stark abgelenkt. Zunächst stellt sich jedoch die Frage: Was sind eigentlich α-Teilchen? α-Teilchen oder Alphastrahlung sind Partikel, die dem Helium sehr ähnlich sind und von radioaktiven Elementen, wie Radium, beim Kernzerfall emittiert werden. Wie wir heute wissen, bestehen sie aus zwei Protonen und zwei Neutronen, aber keinen Elektronen. Es handelt sich daher um zweifach positiv geladene Helium-Ionen. Auch die Alphastrahlung hatte Rutherford bereits kategorisiert und ihr ihren heutigen Namen verpasst (Rutherford 1899). Er wusste so bereits, dass α-Teilchen Heliumkernen entsprechen, die ungefähr die Masse von vier Wasserstoffatomen haben und zweifach positiv geladen sind (Rutherford & Royds 1908).
Auf diesen Experimenten aufbauend wollte Rutherford nun wissen, was passiert, wenn er „leichte“ Atome mit Alphastrahlung beschießt. Insgeheim war es sein eigentliches Ziel die Bestandteile des Atoms zu sprengen. In einem vertraulichen Brief an Niels Bohr beschreibt er seine Fortschritte (Peierls 1988):
“I have got I think results that will ultimately prove of great importance. I wish you were here to talk matters over with. […]. Regard this as private.”
Rutherford vermutete, dass die Alphastrahlung nur bei „leichten“ Elementen, also solchen mit niedriger Ordnungszahl, wie Wasserstoff, Sauerstoff oder Stickstoff, genug Energie hätte, um nahe genug zum Atomkern vordringen und diesen in seine Einzelteile zerlegen zu können.
Um sein Vorhaben in die Tat umzusetzen, überlegte er sich einen geeigneten Versuchsaufbau, der auf den Erfahrungen seiner vorherigen Experimente beruhte. Er ließ sich ein rechteckiges Gehäuse anfertigen, das sowohl eine Strahlungsquelle beherbergen konnte als auch entsprechende Ventile (siehe Abbildung 1 oben) für die Gaszufuhr und Abfuhr besaß.
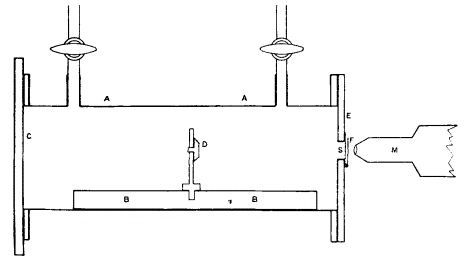
Abbildung1: Rutherfords Versuchsaufbau, A = Messinggehäuse (18x6x2 cm), B = Metallbalken mit Abstandseinstellung, C = Glasplatte, D = radioaktive Scheibe (Radium), E = gewachste Messingplatte, F = Zinksulfid-Schirm, M = Mikroskop, S = rechteckige Öffnung (10×3 mm) mit Metalleinlage (v.a. Silber) (Rutherford 1919a, S. 543ff.)
Über einen entsprechenden metallischen Einsatz in der Öffnung des Gehäuses (siehe Abbildung 1 Buchstabe S) konnte er das Energieniveau der austretenden Alphastrahlung kontrollieren. Je nach Materialart und -dicke passieren nur Alphateilchen eines gewissen Energieniveaus die Öffnung. Dies hängt natürlich von der Positionierung der Strahlungsquelle im Gehäuse ab. Optimalerweise wird die Strahlungsquelle so positioniert, dass nicht die Alphateilchen selbst, sondern nur die zu beobachtenden Gasteilchen die Öffnung passieren. Geladene Teilchen, die die Öffnung schlussendlich durchqueren, können visuell, d.h. mit dem bloßen Auge, über ein Mikroskop gezählt werden. Ionen verursachen beim Auftreten auf einen Zinksulfid-Schirm nämlich ein charakteristisches Funkeln, das Szintillation genannt wird. Positiv geladene Wasserstoffionen, d.h. Protonen, verursachen klar von anderen Ionen unterscheidbare Szintillationen und sind daher gut zu erkennen. Elektronen wurden mit Hilfe eines starken Magnetfeldes abgelenkt (Rutherford 1919a).
Im ersten Teil seines Experiments (Rutherford 1919a) beobachtete Rutherford nun, was passiert, wenn er das Gehäuse mit Wasserstoffgas füllt. Zu seinem Erstaunen nahm die Anzahl der beobachteten Wasserstoffkerne nicht wie erwartet mit dem Abstand zum Zinksulfid-Schirm kontinuierlich ab. Stattdessen beobachtete er eine nahezu konstante Anzahl an Szintillationen, die erst ab einer kritischen Distanz plötzlich und schnell abflauten. Dieser Verlauf war jedoch nur dann zu beobachten, wenn die Alphastrahlung hinreichend energiereich war. Je schwächer das Energieniveau der Alphastrahlung desto eher entsprach der Verlauf dem von der Punktladungstheorie vorhergesagten Verlauf.
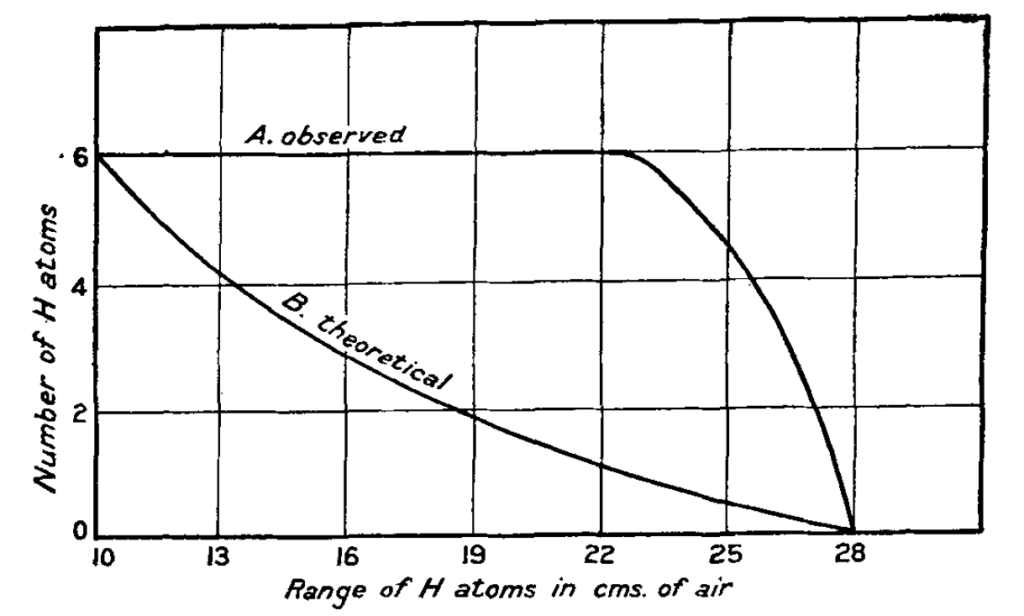
Abbildung 2: Wasserstoff-Szintillationen nach Beschuss von Alphastrahlung in Wasserstoff, A = Versuchsergebnis, B = Theoretische Vorhersage nach der Punktladungstheorie (Rutherford 1919a, S. 549)
-
- die Theorie der Abstoßung von Punktladungen die Verläufe bei Alphastrahlungen niedrigen Energieniveaus gut erklären kann,
- die Anzahl an beobachteten Wasserstoffatomen deutlich höher als erwartet ist, wenn die Alphastrahlung ein bestimmtes Energieniveau überschreitet, und
- in diesem Fall die Wasserstoffatome in die Richtung und auf die gleiche Geschwindigkeit der α-Teilchen beschleunigt werden.
Aus energetischen Betrachtungen schloss Rutherford, dass sich die beiden Kerne bei einem Stoß zwischen einem α‑Teilchen hoher Energie und einem Wasserstoffatom so stark annähern, dass die Größenordnung mit der eines Elektrons vergleichbar ist (Rutherford 1919a). Ausgehend von der Überlegung α-Teilchen seien gleichzusetzen mit Heliumatomen nahm er irrtümlicherweise an, dass α-Teilchen zwei Elektronen besitzen. Dies wiederum brachte ihn auf die Idee, dass die Verformungen durch den Stoß so groß würden, dass die Punktladungstheorie hier versagt und stattdessen eine lokale Anziehung möglich wird. Die kurzzeitige Anziehung hätte so die Kraft die Wasserstoffatome in die Richtung des α-Teilchens zu beschleunigen. Darüber hinaus argumentierte Rutherford, dass die Kombination aus starker Anziehung und Abstoßung die Möglichkeit böte, das α-Teilchen zu sprengen (Rutherford 1919a). Implizit postulierte er somit, dass die beobachteten Wasserstoffatome ebenfalls aus dem α-Teilchen selbst stammen könnten, und mithin den Kernzerfall. Eine für die Wissenschaftswelt geradezu angsteinflößende Implikation, beinhaltete sie doch für viele die mystische Vorstellung der aus der Alchemie bekannten Transmutation.
Auf diesen Erkenntnissen aufbauend untersuchte Rutherford den Beschuss von Luft mit Alphastrahlung (Rutherford 1919c). Wieder waren Szintillationen zu erkennen, die über die Reichweite der α-Teilchen hinausgehen und nicht mit den Vorhersagen der Punktladungstheorie übereinstimmten. Diese Szintillationen schrieb Rutherford den Kollisionen von α-Teilchen mit Stickstoff- sowie Sauerstoffatomen zu, die trotz unterschiedlicher Masse beide eine ähnliche Reichweite aufwiesen. Die Experimente bestätigten nichtsdestotrotz die Vermutung, dass Gasatome in Richtung der α-Teilchen beschleunigt werden, wenn die α-Teilchen genug Energie haben, um nahe genug zum Kern vordringen zu können. Des Weiteren waren auch im Versuchsaufbau an Luft Szintillationen von Atomen großer Reichweite erkennbar, die visuell dem Funkeln von Wasserstoffatomen ähnelten (Rutherford 1919c). Wohlgemerkt der Tatsache, dass Wasserstoff nicht frei in Luft verfügbar ist.
Um dies genauer zu untersuchen, wiederholte Rutherford den Versuchsaufbau aus Abbildung 1 getrennt mit reinem Sauerstoff, Kohlenstoffdioxid und Stickstoff – den Bestandteilen von Luft – als Zwischenmedium (Rutherford 1919d). Die Szintillationen, die den beschleunigten Gasatomen zuzuschreiben und von geringerer Reichweite sind, wurden im Versuchsaufbau durch entsprechende Metallschirme eliminiert, sodass ausschließlich die Szintillationen der relevanten hoch energetischen Atome beobachtet werden konnten. Während bei Flutung des Behälters mit Sauerstoff und Kohlenstoffdioxid nichts Besonderes zu erkennen war, stieg die Anzahl an Szintillationen bei Verwendung von trockener Luft bedeutend an (Rutherford 1919d).
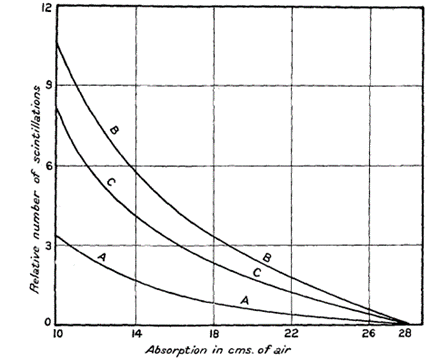
Abbildung 3 Wasserstoff-Szintillationen nach Beschuss von Alphastrahlung in verschiedenen Medien, A = Kohlenstoffdioxid, B = Luft, C = Stickstoff-Effekt (Rutherford 1919d)
Da Intensität und Anzahl vergleichbar mit den Resultaten unter Verwendung eines Gemischs aus Kohlenstoffdioxid und Wasserstoff mit identischem Absorptionsgrad waren, folgerte Rutherford, dass die Szintillationen tatsächlich auf Wasserstoffatome zurückzuführen sind (Rutherford 1919d). Damit sah er seine Vermutung von vorher bestätigt, dass die Kollision von hochenergetischen α‑Teilchen und Gasatomen unter den richtigen Voraussetzungen zu einer Kernspaltung führen könne. Konkret nahm er an, dass durch den Beschuss mit α-Teilchen Wasserstoffkerne vom Stickstoffatom abgespalten würden. Auf dieser Logik beruhend musste das Wasserstoffatom ein konstituierender Bestandteil des Stickstoffatoms sein. Rutherford taufte diesen elementaren Kernbestandteil in Anlehnung an die Hypothese von William Prout (1785-1850), dass alle Atome auf Wasserstoff aufgebaut seien, „Proton“ (Masson 1921).
Stopp! Irgendetwas stimmt hier doch nicht. Sollte es hier nicht um Kernfusion gehen? Rutherford führte die Ergebnisse seiner Experimente auf Zerfallsreaktionen zurück. Wie wir heute wissen, kommt es jedoch beim Beschuss von α-Teilchen und Stickstoff zu einer Fusionsreaktion:
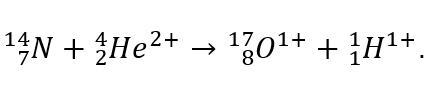
Die dabei auftretenden Sauerstoffisotope korrespondieren mit den von Rutherford detektierten Szintillationen, die in Reichweite denjenigen der freien Sauerstoffatome entsprechen. Der Beschuss mit Alphastrahlung führt also tatsächlich zu einer Kernverschmelzung, bei der Sauerstoff und Protonen freigesetzt werden. Die Protonen konnte Rutherford in seinem Experiment messen. Der Nachweis einer Kernfusionsreaktion im Versuchsaufbau Rutherfords konnte erst sechs Jahre später durch Patrick Blackett (1897-1974), einem Schüler Rutherfords, erbracht werden (Blackett 1925). Und auch wenn Rutherford seine Schlussfolgerungen auf den falschen Tatsachen aufbaute, so müssen wir ihm doch für seinen genialen Weitblick danken, der zur Entdeckung der ersten nuklearen Kernreaktion und des Protons führte.
Autor: NR
Literatur:
Rutherford, Ernest. (1899) ‘Uranium Radiation and the Electrical Conduction Produced by it’, Philosophical Magazine, Fifth Series, Vol. 47, pp. 109-163.
Rutherford, Ernest and Royds, Thomas. (1908) ‘Spectrum of the Radium Emanation’, Philosophical Magazine, Sixth Series, Vol. 16, pp. 313-317.
Rutherford, Ernest. (1911) ‘Scattering of α and β Particles by Matter and the Structure of the Atom’, Philosophical Magazine, Sixth Series, Vol. 21, pp. 669-688.
Rutherford, Ernest. (1919a) ‘Collision of α Particles with Light Atoms. I. Hydrogen’, Philosophical Magazine, Sixth Series, Vol. 37, pp. 537-562.
Rutherford, Ernest. (1919b) ‘Collision of α Particles with Light Atoms. II. Velocity of the Hydrogen Atom’, Philosophical Magazine, Sixth Series, Vol. 37, pp. 562-571.
Rutherford, Ernest. (1919c) ‘Collision of α Particles with Light Atoms. III. Nitrogen and Oxygen Atoms’, Philosophical Magazine, Sixth Series, Vol. 37, pp. 571-581.
Rutherford, Ernest. (1919d) ‘Collision of α Particles with Light Atoms. IV. An Anomalous Effect in Nitrogen’, Philosophical Magazine, Sixth Series, Vol. 37, pp. 581-587.
Masson, Orme. (1921) ‘The Constitution of Atoms’, The Philosophical Magazine, Vol. 41(242), pp. 281-285.
Blackett, P. M. S. (1925) ‘The ejection of protons from nitrogen nuclei, photographed by the Wilson method’, Proceedings of the Royal Society of London, Vol. 107(742), pp. 349–360.
Peierls, Rudolf. (1988) ‘Rutherford and Bohr’, Notes and Records of the Royal Society of London, Vol. 42(2), pp. 229–41.
