Wie sieht ein Photosystem aus? Wie leben mikroskopisch kleine Organismen? Und wie ist eine Zelle eigentlich aufgebaut? Mit unserer Ausstellung BioArt – Aspekte des Lebens widmen wir uns getreu unseres Vereinsmottos der Förderung des Dialogs zwischen Forschung und Kunst. Lass dich inspirieren und sieh Biologie mit neuen Augen! Stattgefunden hat die Ausstellung am 13.06.2025 im Rahmen der Night of Science auf dem Campus Riedberg der Goethe Universität in Frankfurt am Main.
Hier zeigten Frankfurter Forschungsgruppen, wie eindrucksvoll und ästhetisch ihre wissenschaftliche Arbeit sein kann. Entdecke Fotografien, Modelle und Malereien, die direkt aus aktuellen Laborprozessen und naturinspirierten Beobachtungen stammen. So entsteht ein Raum, in dem sich Kunst und Wissenschaft begegnen. Ein Raum zum Staunen, Nachfragen und Weiterdenken.
Du willst dein Wissen zu den Grundlagen der Molekularbiologie auffrischen? Dann schau dir die Artikel der Reihe „Aspekte der Molekularbiologie“ an!
Die Kunstwerke

Licht – Schatten – Struktur
Gestaltet von: Verena Linhard, Monika Linhard, Kathrin Skorodumov, Martin Hähnke, Marco Salustros, Prof. Dr. Harald Schwalbe
Goethe-Universität, Institut für Organische Chemie und Chemische Biologie, Structural Chemistry and Biology/NMR Spectroscopy
Die Installation veranschaulicht die DNA in abstrahierter Form und visualisiert eine Methode der Strukturaufklärung – die Röntgenstrukturanalyse. Mit dieser Methode der Grundlagenforschung gelang es Rosalind Franklin und anderen Wissenschaftler und Wissenschaftlerinnen die DNA zu entschlüsseln.
Die beweglichen Kugeln stellen die einzelnen Atome des Bio-Makromoleküls dar und besitzen eine festgelegte dreidimensionale Anordnung. Der Stoff wird, ähnlich wie bei der Verwendung der Methode der Röntgenstrukturanalyse, von Spotlights angestrahlt. Die zweidimensionalen Schattenbilder, die dabei entstehen, können interpretiert werden, um Information über die dreidimensionale Anordnung der Atome in der DNA zu erhalten.

Zwischen Flug und Wurzel
Gestaltet von: Valentin Graf & Eike Lena Neuschulz
Senckenberg Biodiversität und Klima Forschungszentrum, Interaction Ecology and Climate
Hoch oben in den Alpen trägt der Tannenhäher die Samen der Zirbelkiefer über große Entfernungen und versteckt sie als Wintervorrat im Boden. Aus einigen dieser vergessenen Depots wachsen Jahre später neue Kiefern – langsam, aber widerstandsfähig gegenüber Wind, Schnee und Kälte.
In Ihrer Forschung untersucht die Arbeitsgruppe Interaction Ecology and Climate unter der Leitung von Dr. Eike Lena Neuschulz die Wechselbeziehungen zwischen Pflanzen und Vögeln, insbesondere die Samenausbreitung der Zirbelkiefer durch den Tannenhäher in den Alpen. Besonders faszinierend sind einerseits die weiten Strecken und zahlreichen Flüge, die die Tannenhäher zurücklegen, um ihre Futterdepots anzulegen. Einen starken Kontrast dazu bilden die äußerst langsam wachsenden Kiefern, die an der Baumgrenze den harschen Klimabedingungen trotzen.
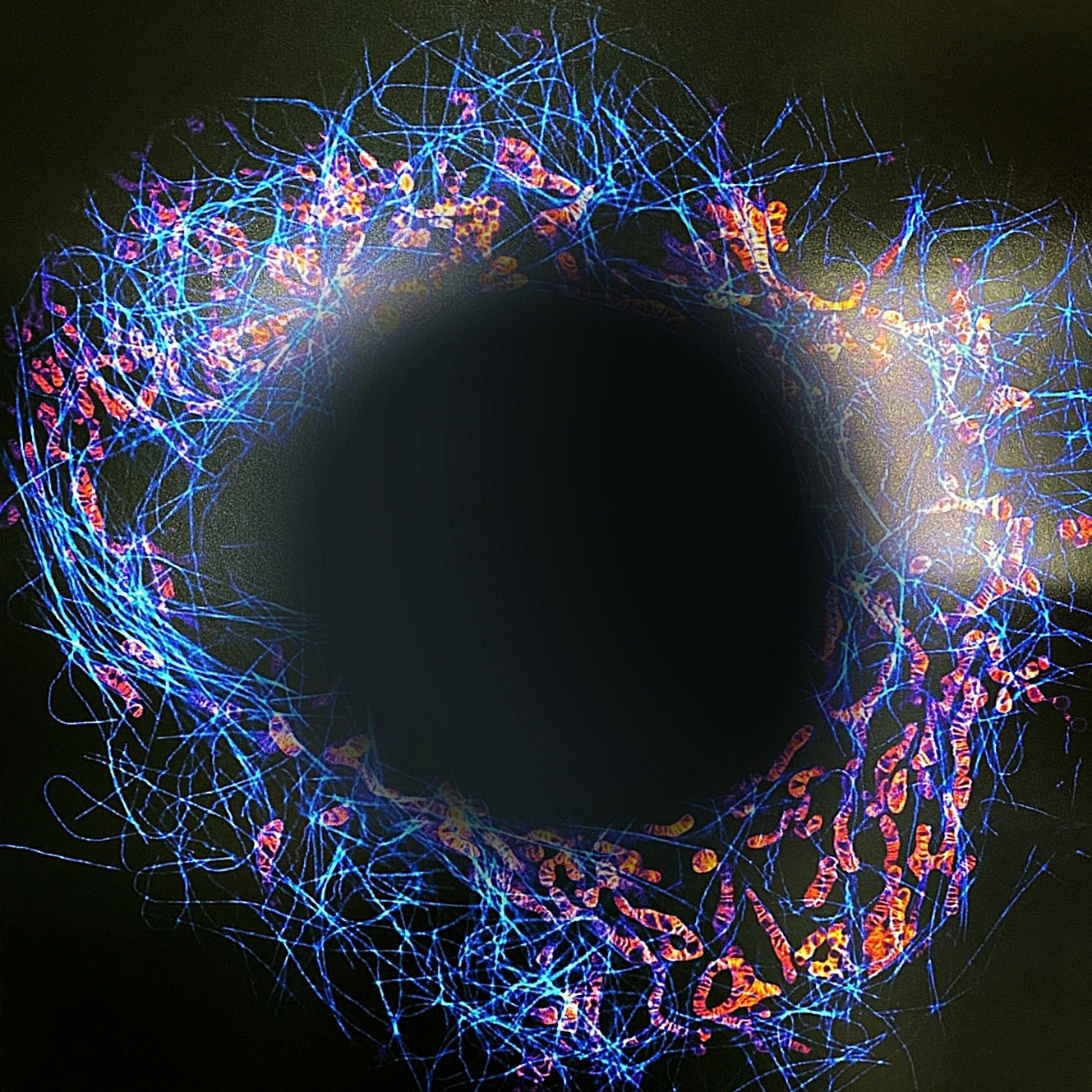
Dual-color live-cell STED
Gestaltet von: Prof. Dr. Till Stephan
Goethe-Universität, Institut für Molekulare Biowissenschaften, Super-Resolution-Mikroskopie von lebenden Zellen
Diese Aufnahme zeigt eine lebende menschliche HeLa-Zelle, dargestellt mithilfe der zweifarbigen STED-Super-Resolution-Mikroskopie. Die Mitochondrien – die Kraftwerke der Zelle – wurden mit dem Fluoreszenzfarbstoff PK Mito Orange markiert (in Rot-Orange) und in 2D mit STED-Nanoskopie abgebildet. Die hohe Auflösung offenbart die lamellenförmige Struktur der Cristae, in denen die Energieproduktion der Zelle stattfindet. In Cyan sind die Mikrotubuli sichtbar – Bestandteile des Cytoskeletts, die der Zelle Stabilität verleihen und als Transportschienen für Organellen dienen. Die STED-Mikroskopie (Stimulated Emission Depletion), mit der diese Aufnahme entstanden ist, wurde 2014 mit dem Nobelpreis für Chemie ausgezeichnet. Sie erlaubt es, dynamische Vorgänge in lebenden Zellen mit bisher unerreichter Präzision sichtbar zu machen.
Die Arbeitsgruppe von Prof. Dr. Till Stephan am Institut für Molekulare Biowissenschaften erforscht, wie die Architektur zellulärer Organellen wie Mitochondrien und endoplasmatisches Retikulum erhalten bleibt und sich flexibel verändert. Im Fokus stehen dabei auch sogenannte „Contact Sites“ – spezialisierte Membranbereiche, an denen Organellen miteinander interagieren und Stoffe austauschen.
Originalabbildung aus: Liu & Stephan et al., Dual-color live-cell STED microscopy of mitochondria and microtubules, PNAS 2022.

Amyloid-Ablagerungen
Gestaltet von: Prof. Dr. Jasmin Hefendehl
Goethe-Universität, Institut für Zellbiologie & Neurowissenschaften, Neurovascular Disorders
Hier sind fein verästelte Hirngefäße (blau) zu erkennen, die von Amyloid (grün) betroffen sind – direkt an den Gefäßwänden und im umliegenden Gewebe. Die intensiv rot gefärbten Astrozyten, zuständig für die Versorgung von Nervenzellen, reagieren sichtbar auf diese krankhafte Veränderung. Die Aufnahme illustriert die Gefäßschädigung bei zerebraler Amyloidangiopathie – einer Erkrankung, die häufig zusammen mit Alzheimer vorkommt.

Leuchtende Lebensadern
Gestaltet von: Mathieu Preussner & Prof. Dr. Virginie Lecaudey
Goethe-Universität, Institut für Zellbiologie & Neurowissenschaften, Developmental Biology of Vertebrates
Feine, leuchtende Linien durchziehen dieses Bild: Es zeigt die Blutgefäße in den Kiemen eines Zebrafisches. Sichtbar werden sie durch ein fluoreszierendes Protein, das gezielt in sogenannte Endothelzellen eingebracht wurde – die Zellen, aus denen Blutgefäße bestehen. Mit Hilfe genetisch veränderter Zebrafische erforscht die Arbeitsgruppe Arbeitsgruppe Developmental Biology of Vertebrates unter der Leitung von Prof. Dr. Virginie Lecaudey, wie solche Gefäßsysteme entstehen. Dabei stehen vor allem die Gene im Fokus, die die Entwicklung dieser Strukturen steuern. Denn: Die Bildung von Blutgefäßen ist nicht nur ein lebenswichtiger Vorgang in gesunden Organismen, sondern spielt auch bei Krebs eine zentrale Rolle. Tumore benötigen Sauerstoff und Nährstoffe – die sie über neu gebildete Gefäße erhalten.
Der Zebrafisch ist dabei ein besonders geeignetes Modell: Seine Kiemen besitzen die erstaunliche Fähigkeit, sich nach einer Schädigung vollständig zu regenerieren – eine Fähigkeit, die dem Menschen fehlt. So erlaubt dieses Tiermodell wertvolle Einblicke in die Regeneration, die Gefäßentwicklung und die Mechanismen schwerer Erkrankungen.

Molekülmodell einer RNA-Struktur
Gestaltet von: Verena Linhard, Monika Linhard, Kathrin Skorodumov, Martin Hähnke, Marco Salustros, Prof. Dr. Harald Schwalbe
Goethe-Universität, Institut für Organische Chemie und Chemische Biologie, Structural Chemistry and Biology/NMR Spectroscopy
Molekülmodell einer RNA-Struktur des viralen COVID Erregers SARS-CoV-2 / Struktur berechnet mithilfe von experimentellen Kernspin-Resonanz Daten. 3D-Druck aus Polymilchsäure
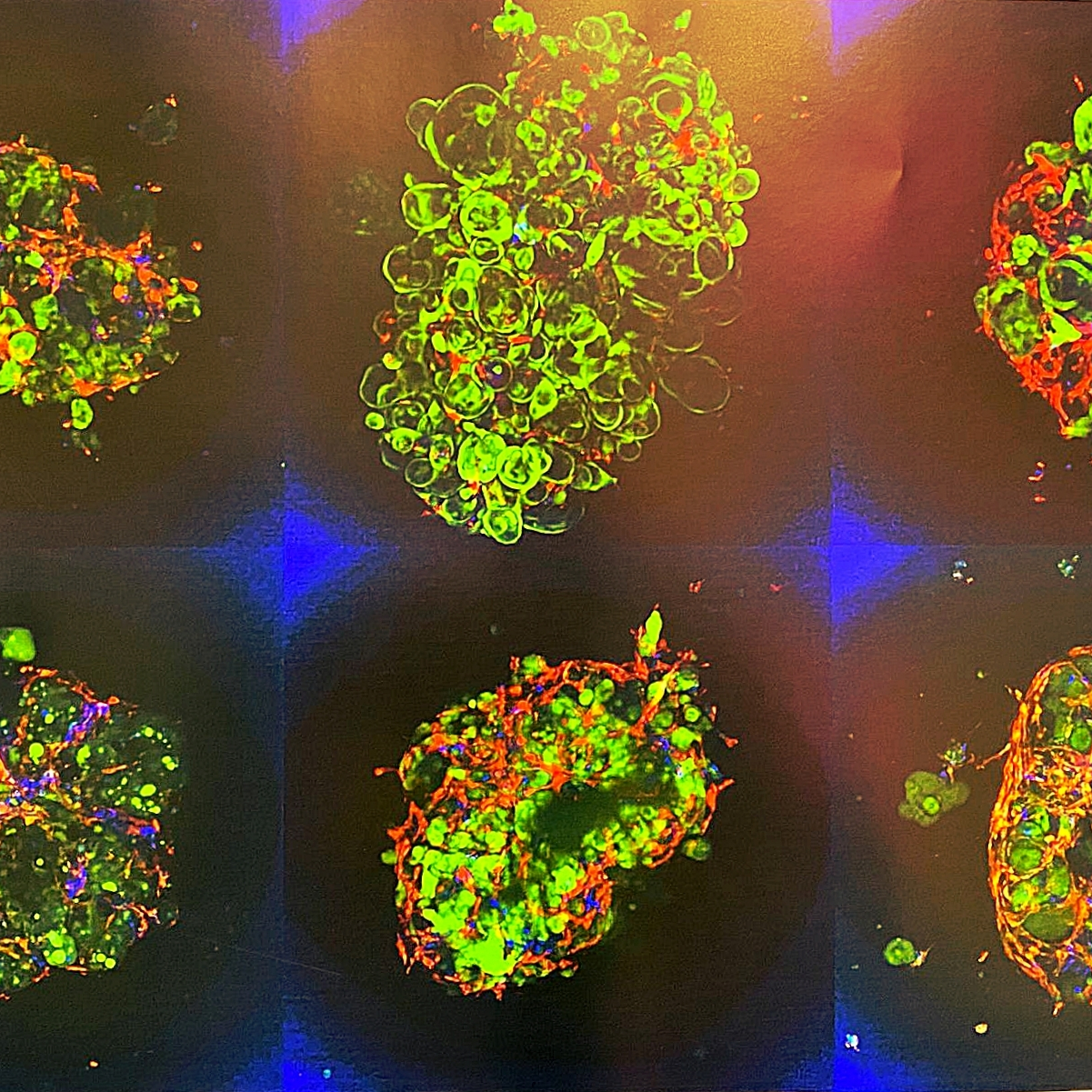
The Universe of Colon Cancer
Gestaltet von: Maria Correia da Silva Melo & Prof. Dr. Henner Farin
Georg-Speyer-Haus, Experimentelle Modelle für die Mikroumgebung beim Darmkrebs
Was auf den ersten Blick wie ein fernes Universum wirkt, ist in Wirklichkeit ein Mikrokosmos menschlicher Zellarchitektur: Aus Tumorgewebe von 6 verschiedenen Patienten und Patientinnen wurden sogenannte „Organoide“ des kolorektalen Karzinoms (grün) kultiviert und mit Fibroblasten (rot) sowie Gefäßzellen (blau) kombiniert. Die so entstehenden „Assembloide“ bilden komplexe Strukturen und bilden so ein dreidimensionales Modell der Tumorumgebung im Labor nach.
Die Forschungsgruppe Experimentelle Modelle für die Mikroumgebung beim Darmkrebs unter der Leitung von Prof. Dr. Henner Farin am Georg-Speyer-Haus erforscht, wie verschiedene Zelltypen im Umfeld von Darmtumoren miteinander kommunizieren. Durch moderne Organoid-Technologie schaffen sie realistische Labormodelle, um zu verstehen, wie die Mikroumgebung den Krankheitsverlauf beeinflusst, und wie daraus personalisierte Therapien entwickelt werden können.
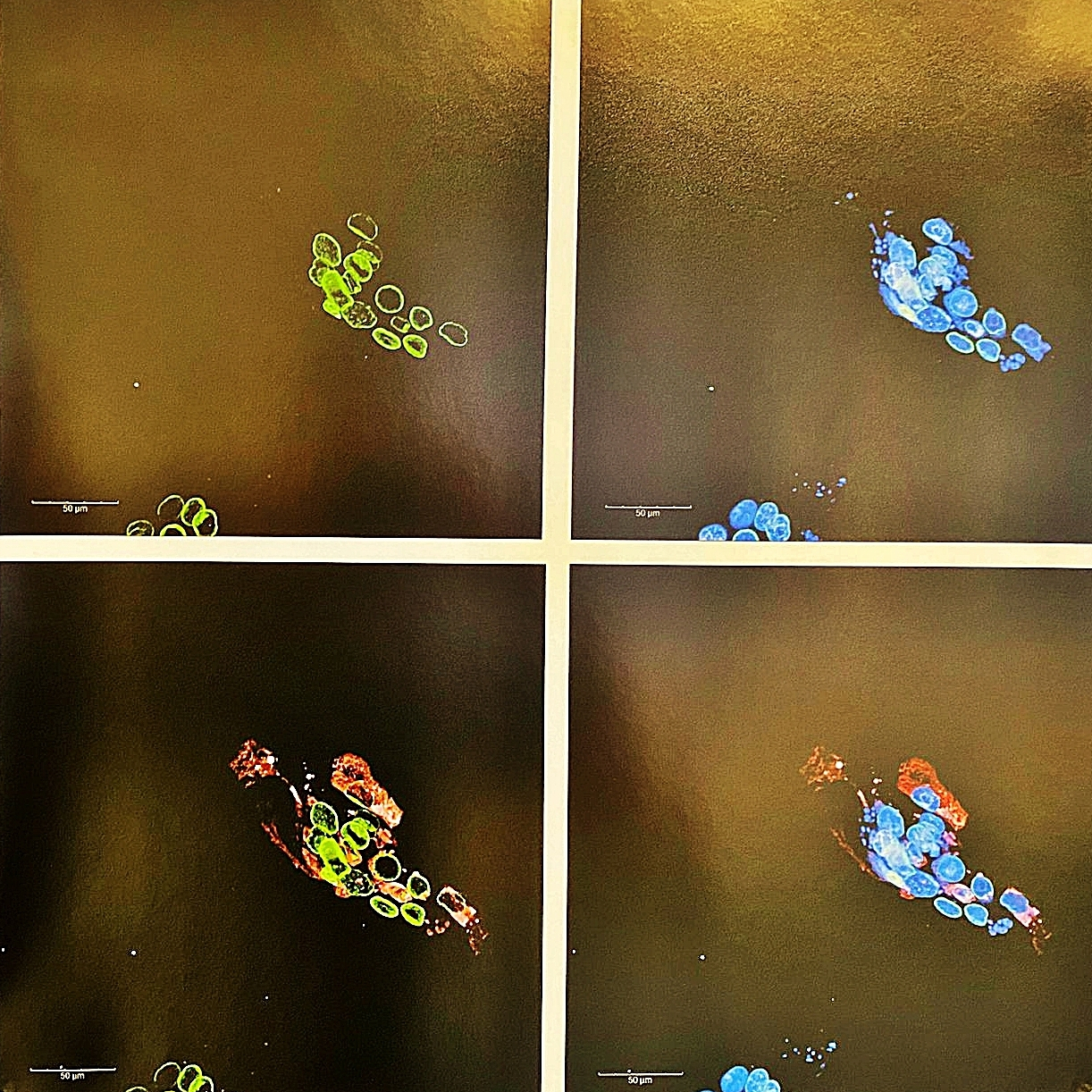
MPox-Infektion
Gestaltet von: Prof. Dr. Denisa Bojkova, Emma Torbica, Matthias Denkewitz, Lena Stegmann
Goethe-Universität, Institut für Medizinische Virologie
Die Aufnahme zeigt eine MPox-(Affenpocken-)Infektion in menschlichen Hautzellen, auch Keratinozyten genannt. In Grün ist die Zellkernmembran markiert, in Blau der Zellkern selbst – und in Rot die virale Infektion. Besonders auffällig sind die sogenannten „Viral Factories“: blau gefärbte Strukturen im Zytoplasma, außerhalb des Zellkerns. Diese Virusfabriken sind typisch für MPox – anders als viele andere DNA-Viren vermehrt sich MPox nicht im Zellkern, sondern in diesen zytoplasmatischen Kompartimenten. Die hier sichtbare Darstellung macht die feinen Details der Virus-Wirt-Interaktion auf zellulärer Ebene sichtbar.
Am Institut für Medizinische Virologie untersucht die Arbeitsgruppe um Prof. Dr. Denisa Bojkova die Schnittstelle zwischen Virus und Wirtszelle. In verschiedenen zellulären Modellen mit unterschiedlicher Organspezifität analysieren sie, wie Viren menschliche Zellen infizieren und manipulieren. Darüber hinaus suchen sie gezielt nach antiviralen Wirkstoffen gegen eine Vielzahl von Erregern zu suchen.
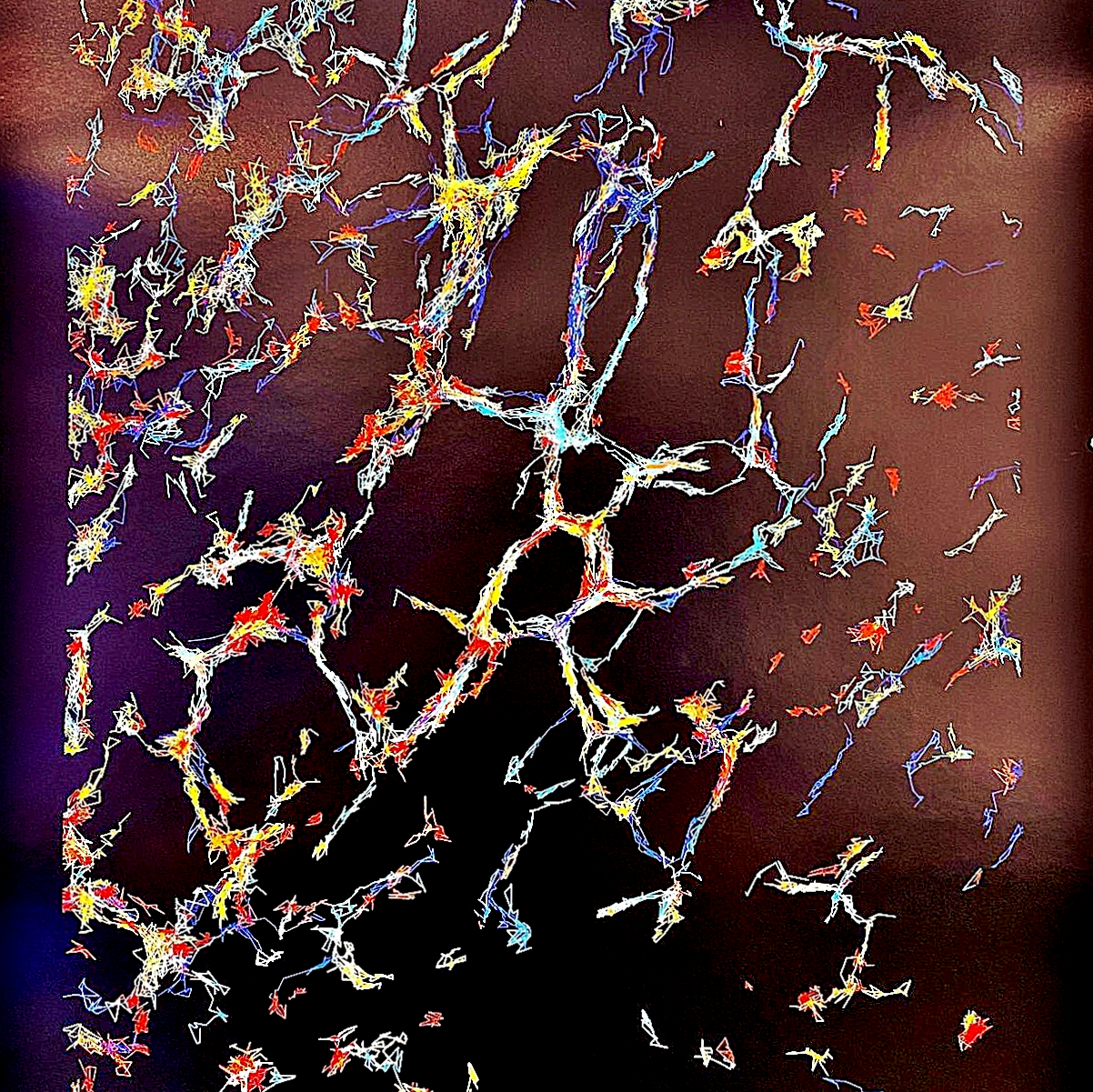
Zelluläre Highways
Gestaltet von: Claudia Catapano & Prof. Dr. Mike Heilemann
Goethe-Universität, Institut für Physikalische und Theoretische Chemie, Single Molecule Biophysics
Tief im Inneren der Zelle existiert ein Netzwerk von unfassbarer Dynamik: das endoplasmatische Retikulum (ER). Es bildet ein verzweigtes Röhrensystem – ein zellulärer „Verkehrsknotenpunkt“, in dem Proteine hergestellt, verarbeitet und transportiert werden. In dem Bild „Zelluläre Highways“ sind winzige Proteinmoleküle zu sehen, die sich durch die Membranstruktur des ER bewegen – wie Autos auf Autobahnen. Die Linien zeigen ihre Wege, und ihre Farben verraten die Geschwindigkeit: Kühle Töne stehen für schnelles Vorankommen, warme Farben für langsames Durchqueren dichter Zellregionen. Solche Einblicke verdanken wir der Super-Resolution-Mikroskopie, einer Technologie, die die gleichnamige Arbeitsgruppe unter der Leitung von Prof. Dr. Mike Heilemann ständig weiterentwickelt. Damit wollen sie die Organisation und Dynamik biomolekularer Netzwerke in Zellen sichtbar machen und so die Grundlagen lebendiger Systeme besser verstehen.
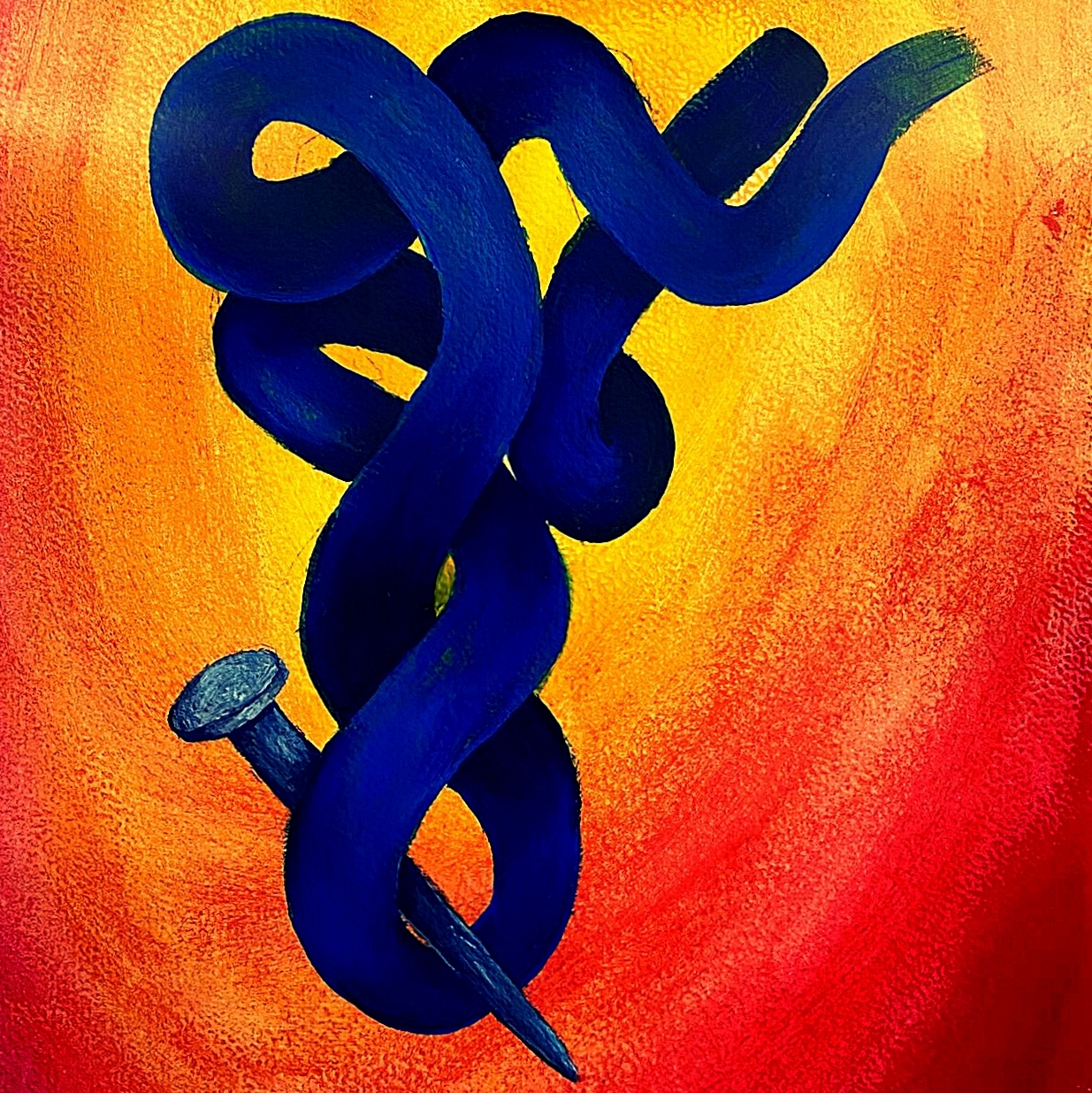
Genagelte tRNA
Gestaltet von: Prof. Dr. Stefanie Kaiser
Goethe-Universität, Institut für Pharmazeutische Chemie, Massspectronomy
Die mittels Acryls auf Papier gemalte tRNA – ein zentrales Molekül der Eiweißherstellung – trägt symbolisch einen Nagel. Dieser steht für eine innovative Technologie namens NAIL-MS (Nucleic Acid Isotope Labeling coupled Mass Spectrometry), die in der Arbeitsgruppe Massspectronomy unter der Leitung von Prof. Dr. Stefanie Kaiser entwickelt wurde.
tRNA-Moleküle transportieren Aminosäuren zu den Ribosomen, wo anhand der Boten-RNA (mRNA) Proteine gebaut werden. Damit die tRNA diese Aufgabe korrekt erfüllt, wird sie im Körper an bestimmten Stellen chemisch modifiziert. Diese Modifikationen stabilisieren ihre L-förmige Struktur und sind entscheidend für ihre Funktion. Ein Ungleichgewicht – sei es zu wenig oder zu viel Modifikation – kann zu Krankheiten führen. Um solche Zusammenhänge besser zu verstehen, ermöglicht NAIL-MS die präzise Messung dieser tRNA-Modifikationen in lebenden Zellen. Das „Genageltsein“ der tRNA im Kunstwerk steht damit stellvertretend für die Fähigkeit der Methode, molekulare Prozesse mit höchster Genauigkeit „festzunageln“ und sichtbar zu machen.
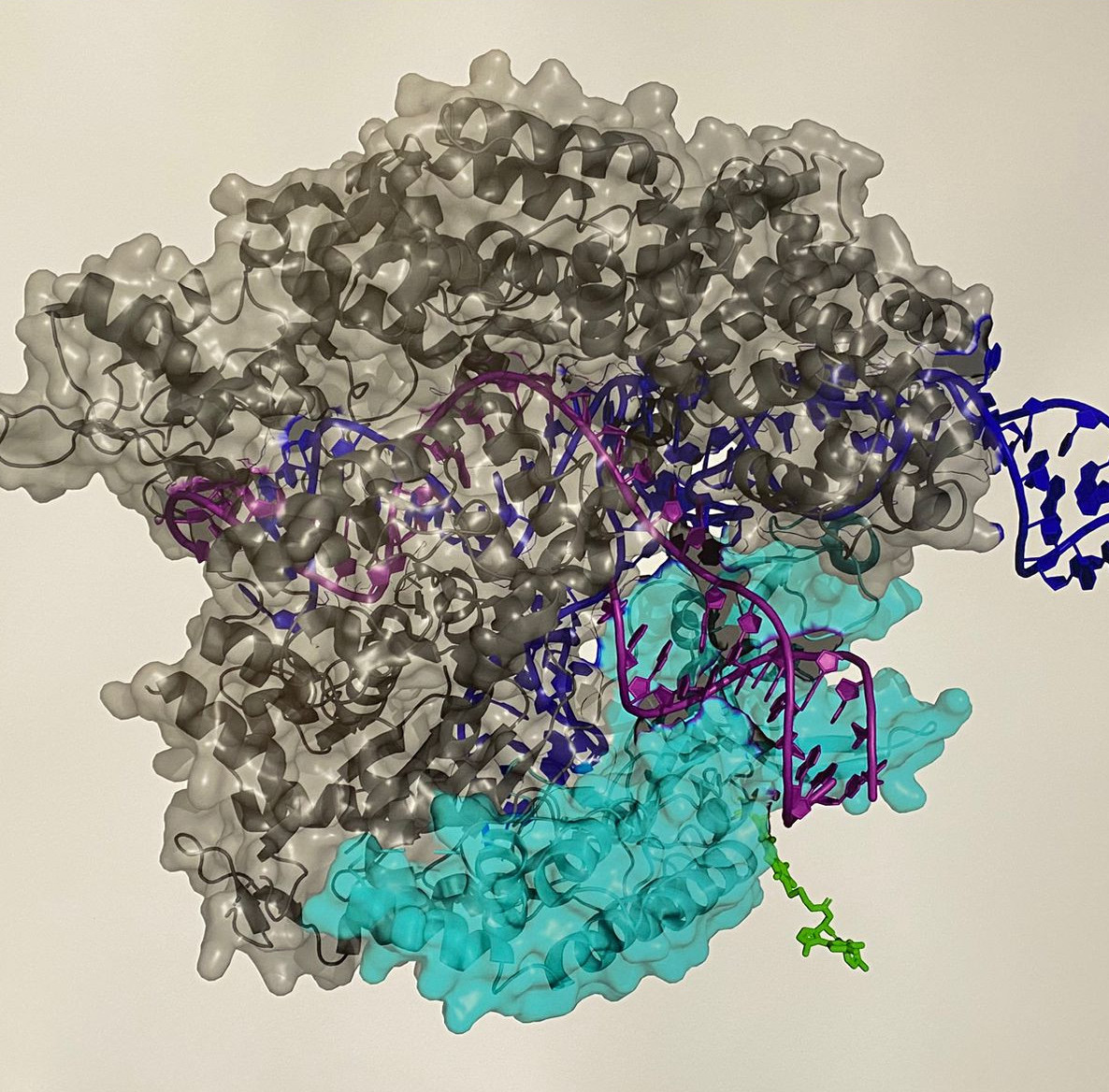
CRISPR Precise
Gestaltet von: Dr. Xinlai Cheng & Mukaddes Altinbay
Buchmann Institute for Molecular Life Sciences, Chemical Biology
Wie ein molekularer GPS-Sender zielt das CRISPR/Cas9-System auf MYC – ein Gen, das bei vielen Krebserkrankungen überaktiv ist und bislang als „nicht medikamentös angreifbar“ galt. Die Visualisierung zeigt, wie diese präzise Gensteuerung durch die Anbindung des Wirkstoffs JQ1 (grün hervorgehoben) weiter verstärkt werden kann. JQ1 bindet gezielt an das Protein BRD4, das natürliche Signale in der Nähe von MYC erkennt – ein strategischer Doppelschlag gegen krebsfördernde Genaktivität.
Die Arbeitsgruppe Chemical Biology unter der Leitung von Dr. Xinlai Cheng beschäftigt sich mit der Entwicklung neuartiger Wirkstoffe gegen bislang als „undruggable“ geltende Proteine. Ihr Ziel: Die Erweiterung des „druggable proteome“, also der Menge an krankheitsrelevanten Proteinen, die durch Medikamente gezielt beeinflusst werden können. Dazu kombiniert das Team Methoden der organischen Chemie mit modernsten biotechnologischen Werkzeugen – von RNA-Sequenzierung über Proteom-Analysen bis hin zur gezielten Genmanipulation.
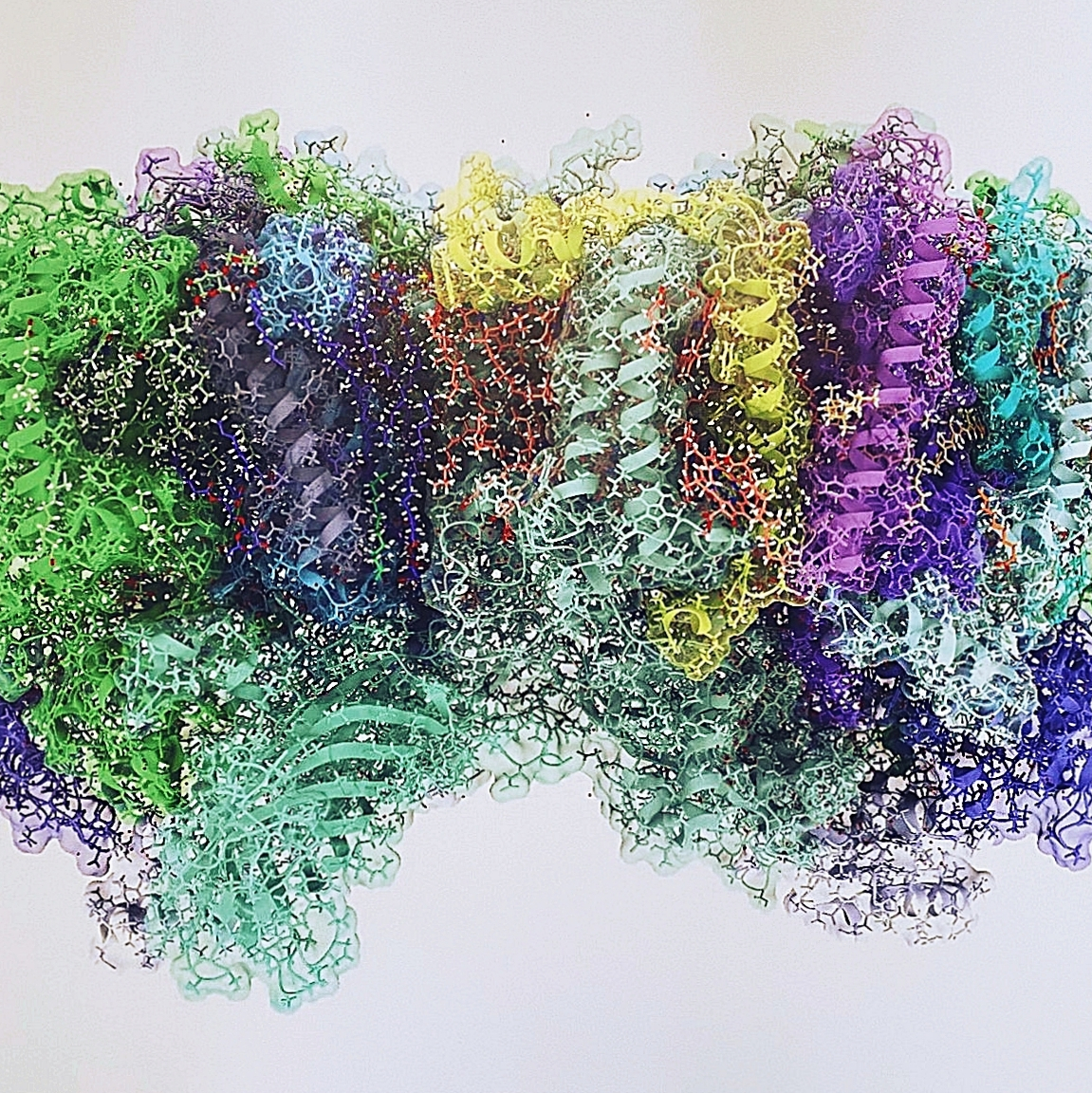
Photosystem II
Gestaltet von: Stefan Frühschulz & Dr. Rana Hussein Ali
Goethe-Universität, Institut für Biochemie, Structural Biology of Membrane Associated Photosynthetic Proteins
Das Photosystem II (PSII) ist der erste zentrale Protein-Komplex der Photosynthese und das einzige bekannte biologische System, das Wasser mithilfe von Licht in atembaren Sauerstoff umwandeln kann. Die hier dargestellte Struktur – entschlüsselt von Dr. Rana Hussein Ali und ihren Kollegen und Koleginnen mithilfe modernster Kryo-Elektronenmikroskopie (Rana Hussein et al., 2024 in Science) – zeigt das Photosystem II (PSII) in atomarer Auflösung. Das Verständnis dieses großen Protein-Komplexes öffnet die Tür für vielfältige Anwendungsmöglichkeiten: von der Herstellung grünen Wasserstoffs aus Licht und Wasser, über die Entwicklung semi-biologischer Solarpaneele, bis hin zu neuen, umweltschonenderen Herbiziden.
Die Arbeitsgruppe Structural Biology of Membrane-Associated Photosynthetic Proteins am Institut für Biochemie erforscht die Struktur und Funktion membrangebundener Proteinkomplexe der Photosynthese. Mithilfe modernster Methoden wie XFEL-Kristallografie, Kryo-EM und Spektroskopie werden dynamische Prozesse der biologischen Energieumwandlung sichtbar gemacht. Das Ziel ist: aus den Prinzipien der Natur zukunftsfähige Technologien zu entwickeln.
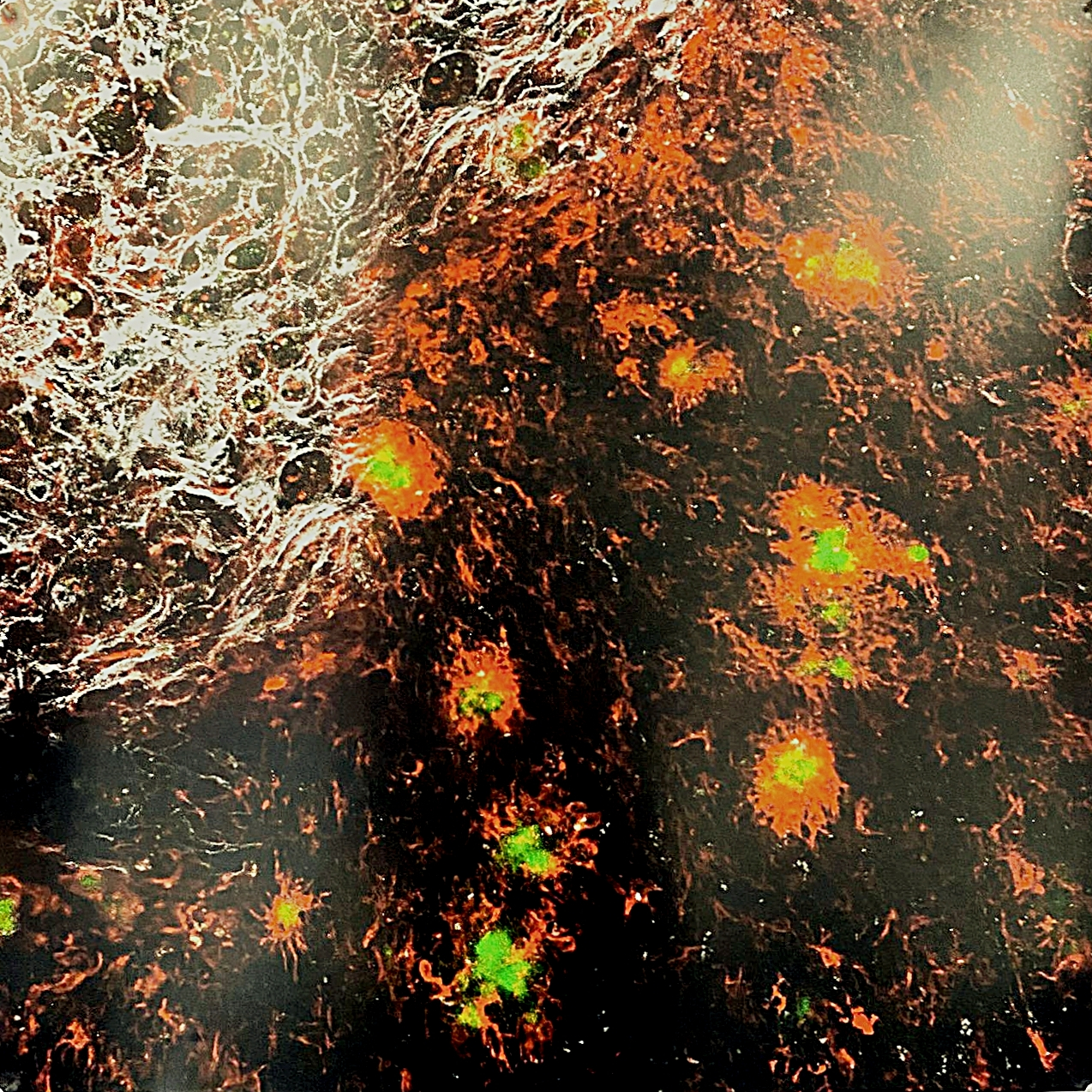
Immunreaktion im Gehirn
Gestaltet von: Prof. Dr. Jasmin Hefendehl
Goethe-Universität, Institut für Zellbiologie & Neurowissenschaften, Neurovascular Disorders
Zu sehen ist ein Gehirnschnitt nach einem Schlaganfall mit gleichzeitiger Amyloid-Ablagerung zu sehen – typisch für die Alzheimer-Erkrankung. Grün zeigt Amyloid-Plaques rund um das Infarktareal, weiß markiert Zellen im geschädigten Zentrum. Rote Strukturen machen die Aktivität der Mikroglia sichtbar, der Immunzellen des Gehirns. Die Kombination aus Schlaganfall und Amyloid verdeutlicht ein oft unterschätztes Krankheitsbild: das gleichzeitige Auftreten von Alzheimer und vaskulärer Demenz
Die Arbeitsgruppe Neurovascular Disorders unter der Leitung von Prof. Dr. Jasmin Hefendehl untersucht das komplexe Zusammenspiel von Gefäßen, Immunzellen und Nervenzellen bei neurodegenerativen Erkrankungen. Im Fokus stehen die Störungen der sogenannten neurovaskulären Einheit – also dem funktionellen Zusammenschluss aus Neuronen, Gefäßen, Astrozyten und Mikroglia. Ziel der Forschung ist es, mithilfe moderner Bildgebung und molekularbiologischer Methoden neue Mechanismen der Krankheitsentstehung zu verstehen und Ansatzpunkte für Diagnose und Therapie zu finden.
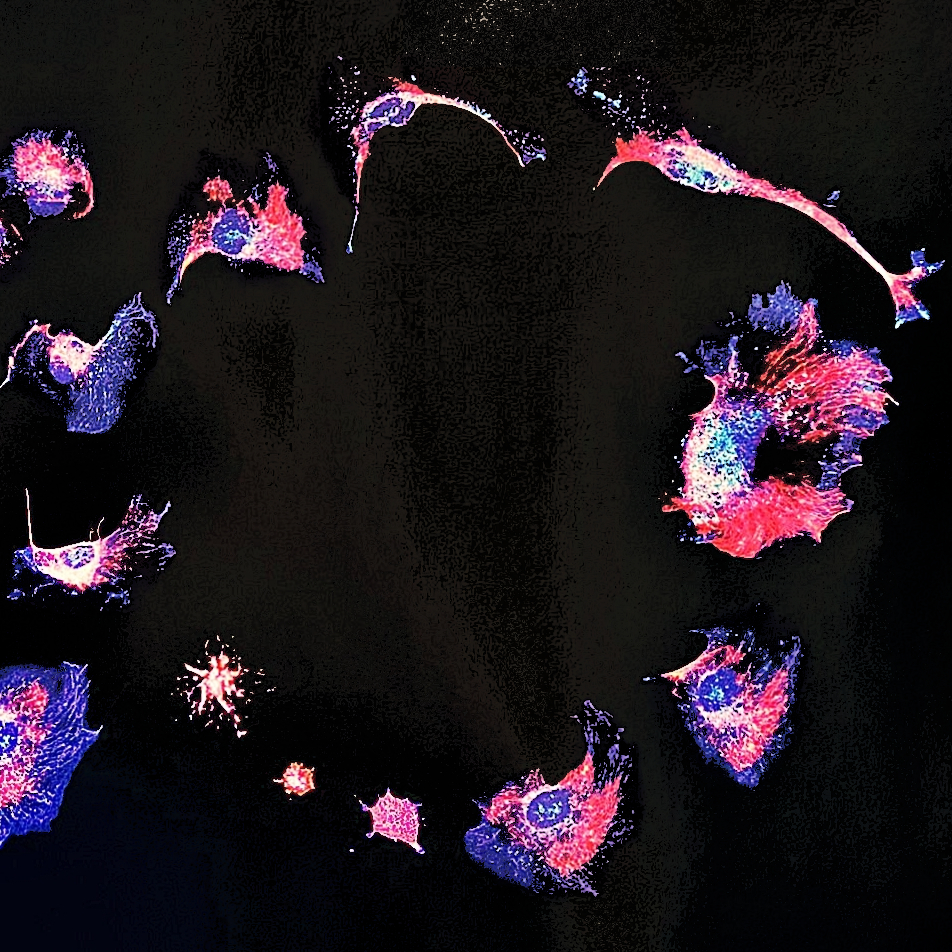
The Cycle of Life
Gestaltet von: Claudia Catapano & Prof. Dr. Mike Heilemann
Goethe-Universität, Institut für Physikalische und Theoretische Chemie, Single Molecule Biophysics
Das Bild „The Cycle of Life“ zeigt den Kreislauf des Lebens: Krebszellen, die sich teilen, vermehren – und auch sterben. Die hier gezeigten Zellen stammen aus einem Gebärmutterhalskarzinom der US-Amerikanerin Henrietta Lacks. Ihre sogenannten HeLa-Zellen wurden am 9. Februar 1951 ohne ihr Wissen entnommen – und leben bis heute in zahllosen Forschungslaboren weltweit weiter. Sie teilen sich unkontrolliert und gelten als biologisch „unsterblich“. Die Aufnahme wurde mittels Fluoreszenzmikroskopie erstellt und erlaubt einen Einblick in zelluläre Prozesse, die oft im Verborgenen ablaufen, aber die Grundlage für medizinische Forschung und Therapieentwicklung bilden
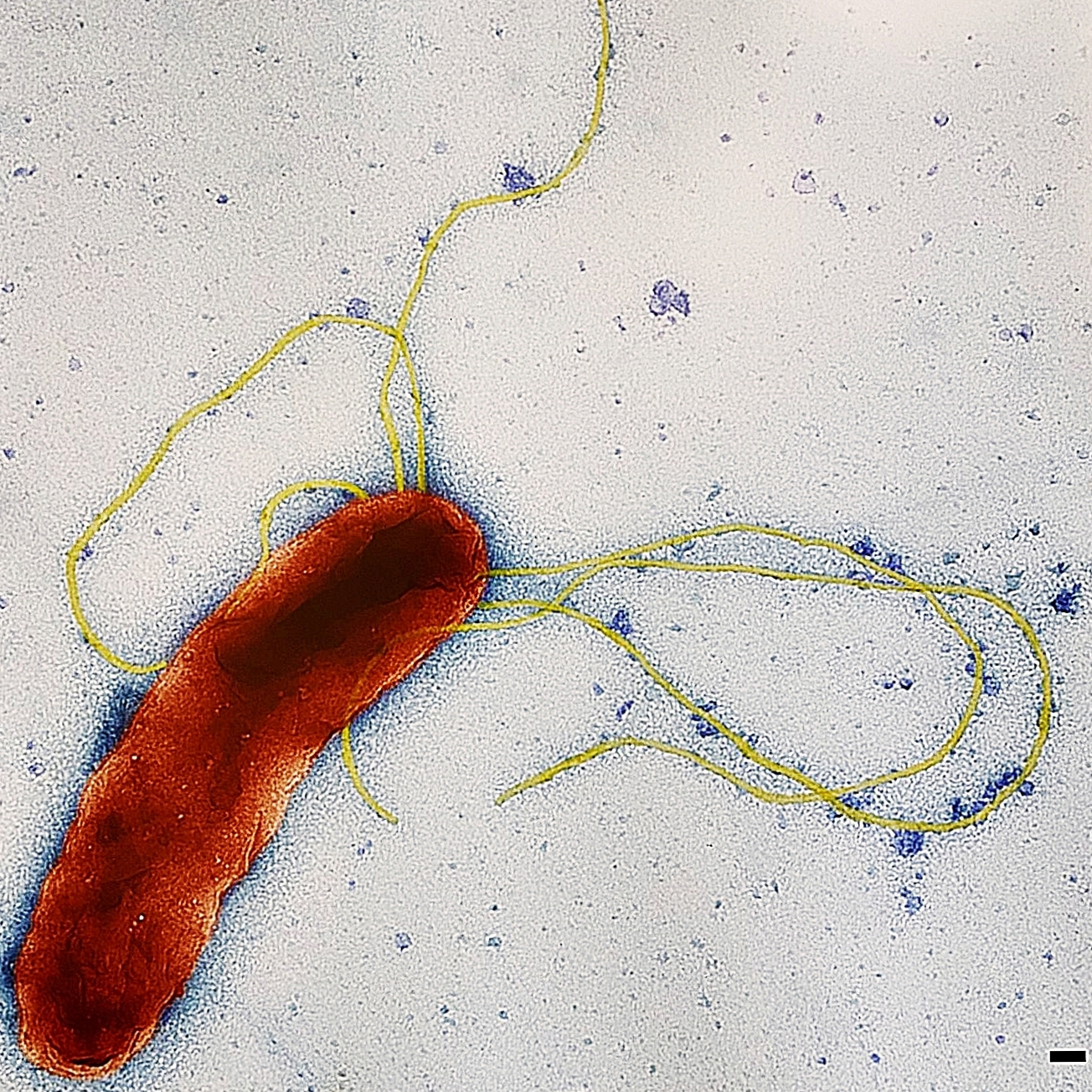
Bartonella bacilliformis
Gestaltet von: Prof. Dr.. Volkhard A. J. Kempf
Goethe-Universität, Institut für Medizinische Mikrobiologie und Krankenhaushygiene
Dieses eindrucksvolle Bild zeigt eine kolorierte Raster-Elektronenmikroskopie-Aufnahme des tropischen Bakteriums Bartonella bacilliformis, einem Erreger, der zu den sogenannten „neglected tropical pathogens“ zählt. Bartonella bacilliformis kommt vor allem in den Hochlagen der Anden Südamerikas, insbesondere in Peru, vor und wird durch Sandmücken übertragen. Beim Menschen kann es zu einer schweren Infektion führen, dem „Oroya-Fieber“, das durch eine massive Zerstörung der roten Blutkörperchen (hämolytische Anämie) gekennzeichnet ist. Unbehandelt endet diese Krankheit in bis zu 90 % der Fälle tödlich – damit zählt sie zu den gefährlichsten bakteriellen Infektionen weltweit.
Auf dem Bild sind deutlich die fünf Flagellen (Geißeln) zu erkennen, die dem Bakterium seine Beweglichkeit verleihen. Diese Strukturen sind essenziell für die Fähigkeit des Erregers, sich im menschlichen Körper fortzubewegen und Zellen zu infizieren.
Originalabbildung aus: Garcia-Quintanilla et al., Carrion’s disease: more than a neglected disease, Parasites & Vectors 2019.
Teilnehmende Forschungsgruppen: Structural Chemistry and Biology/NMR Spectroscopy (Verena Linhard, Monika Linhard, Kathrin Skorodumov, Martin Hähnke, Marco Salustros, Prof. Dr. Harald Schwalbe), Chemical Biology (Dr. Xinlai Cheng, Mukaddes Altinbay), Interaction Ecology and Climate (Valentin Graf, Dr. Eike Lena Neuschulz), Forschungsgruppe für Experimentelle Modelle für die Mikroumgebung beim Darmkrebs (Maria Correia da Silva Melo, Prof. Dr. Henner Farin), Structural Biology of Membrane Associated Photosynthetic Proteins (Stefan Frühschulz, Dr. Rana Hussein Ali), Super-Resolution-Mikroskopie von lebenden Zellen (Prof. Dr. Till Stephan), Medizinische Virologie (Emma Torbica, Matthias Denkewitz, Lena Stegmann, Prof. Dr. Denisa Bojkova), Neurovascular Disorders (Prof. Dr. Jasmin Hefendehl), Single Molecule Biophysics (Claudia Catapano, Prof. Dr. Mike Heilemann), Developmental Biology of Vertebrates (Mathieu Preussner, Prof. Dr. Virginie Lecaudey), Kaiser Isotope Lab (Prof. Dr. Stefanie Kaiser), Krankenhaushygiene (Prof. Dr. Volkhard A. J. Kempf).
Wir bedanken uns bei allen teilnehmenden Forschungsgruppen, dem Organisations-Team der Night of Science e.V., M. Florschütz & H. Gottschalk für den Aufbau und die Kuration und bei allen Besuchern und Besucherinnen für den großartigen Abend!





