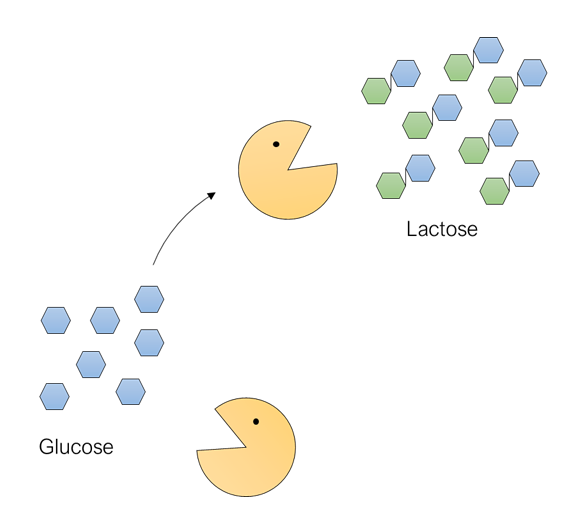
Wir befinden uns im Jahre 1960. Wenige Jahre zuvor wurde die DNA als Träger der genetischen Erbinformation entdeckt (1944 – Oswald T. Avery), die Struktur dieser durch James Watson und Francis Crick mit unerlässlicher Hilfe von Rosalind Franklin und Maurice Willkins gelöst (1953) und deren Art der Replikation durch Matthew Meselson und Franklin Stahl entdeckt (1958). Die Molekularbiologie steht nun nicht mehr in den Kinderschuhen, sondern wächst rasant mit einer immer größeren Anzahl an WissenschaftlerInnen auf der ganzen Welt, welche sich mit Fragen rund um die biologische Rolle der DNA und ihre Verbindung zum Leben beschäftigen. So wurde allgemein angenommen, dass einzelne Abschnitte der DNA die Information für den Aufbau und die Zusammensetzung von bestimmten Proteinen beinhalten. Diese Abschnitte werden auch als Gene definiert und das Speichern von Information als Codieren bezeichnet (Gamow, 1954; Watson, 1963; Crick, 1964). Als Verbindungsstück zwischen der DNA als statischer Informationsspeicher und den agilen Proteinen wurde ein weiteres Molekül, die Messenger-Ribonukleinsäure (mRNA) angenommen. Viele Arbeitsgruppen arbeiteten zu dieser Zeit an Bakterien, da sie im Vergleich zu Pflanzen oder Tieren für die Molekularbiologie leichter zu handhaben sind. Eines der in den Laboren am weitesten verbreiteten Bakterien war und ist immer noch das Bakterium Escherichia coli (E. coli). Um es zu vermehren und eine ausreichende Menge an Biomasse (Menge an organischem Material, z.B. ein gewisses Gewicht an Bakterien) zu produzieren, braucht man es lediglich in ein mit flüssigem Nährmedium (eine Flüssigkeit, welche alle Nähstoffe für das Wachstum von Bakterien beinhaltet) gefüllten Behälter zu geben und zu warten. Das exponentielle Wachstum des Bakteriums lässt sich bereits nach einigen Stunden durch die Trübung des Mediums beobachten. Unter optimalen Bedingungen verdoppelt sich die Anzahl an E. coli Bakterien alle 20 min. Optimal ist eine Temperatur von 37°C und eine ausreichende Versorgung mit Nährstoffen. Bei Zweiterem spielt die Quelle an Kohlenhydraten (=Zucker) eine entscheidende Rolle, so nehmen sie bevorzugt Glucose auf, können aber auch andere Zucker zersetzen und daraus Energie gewinnen. Ein Beispiel: Befinden sich in dem Nährmedium sowohl Glucose (ein Einfachzucker bzw. „Monosacharid“) als auch Lactose (einem Zweifachzucker bzw. „Disacharid“, welches aus den Monosacchariden Glucose und Galactose aufgebaut ist) als Zucker-Quelle, nimmt ein E. coli Bakterium bevorzugt die Glucose auf. Erst wenn diese verbraucht ist, bedient es sich an der Lactose. Ähnlich wie wir Menschen hat auch das Bakterium eine Art „Lieblingsessen“ und greift erst zu einer Alternative, wenn dessen Leibspeise nicht zur Verfügung steht. Um Glucose abzubauen und Energie zu gewinnen, werden bestimmte Enzyme benötigt. Der Abbau von Lactose hingegen erfordert zusätzliche Enzyme, welche das Disaccharid in seine Bestandteile (die Monosacchariden Glucose und Galactose) spalten, welche von da an, denselben Prozess zur Energiegewinnung durchlaufen. Es würde sich demnach für das Bakterium energetisch betrachtet lohnen, wenn es die zusätzlichen Enzyme zum Abbau der Lactose erst synthetisieren (=herstellen) muss, wenn diese auch benötigt werden. Sind die Bakterien nun gezwungen von Glucose auf Lactose als Zucker umzusteigen, müssen jedoch die zusätzlichen Enzyme synthetisiert werden, welche die Energiegewinnung auf den Abbau von Lactose ausrichten. Ein solcher Vorgang wurde von WissenschaftlerInnen häufig beobachtet und man gab diesem Phänomen die Bezeichnung „Enzymadaptation“. Die Theorie der Enzymadaptation geht im Allgemeinen davon aus, dass sich die Anzahl der in einer Zelle befindlichen Enzyme in Abhängigkeit eines Umweltreizes verändern kann (Duclaux 1898, Dienert, 1900). An dem Glucose/Lactose-Beispiel von vorhin würde es bedeuten: Befindet sich Glucose im Medium, kommen die Enzyme zum Abbau von Glucose häufig in der Zelle vor und die für den Abbau von Lactose in sehr geringen Mengen. Ist aber nur Lactose im Medium vorhanden, erhöht sich die Menge an den zusätzlich benötigten Enzymen für den Abbau von Lactose. Die Lactose induziert also in diesem System ihren eigenen Abbau und wird deswegen hier auch als „Inducer“ bezeichnet.
Lange ging man davon aus, dass alle Proteine in einem Organismus dauerhaft gebildet werden. Dieser Vorgang wird auch als Gen-Expression bezeichnet und die ständige Expression als konstitutiv. Dass bestimmte Gene (z.B. die zum Abbau von Lactose) aber nur unter bestimmten Bedingungen exprimiert werden, war lange unvorstellbar, weswegen die Theorie der enzymatischen Adaptation von vielen WissenschaftlerInnen abgelehnt wurde. Die beiden französischen Wissenschaftler Francis Jacob und Jaques Lucien Monod waren es jedoch, welche eine außergewöhnliche Hypothese über die Regulierung der Expression bestimmter Gene unter bestimmten Umwelteinflüssen aufstellten und diese mit Experimenten stützen konnten.
Francis Jacob wurde am 17. Juni 1920 in Nancy (Frankreich) geboren. In Paris fing er im Jahre 1939 ein Studium der Medizin an, welches er unterbrochen durch den Dienst als Sanitätsoffizier im Zweiten Weltkrieg im Jahre 1951 beendete. Danach schloss er sich am Pariser Institut Pasteur der Arbeitsgruppe um André Lwoff, einem der zu der Zeit führenden Mikrobiologen und Virologen seiner Zeit, an. Dort lernte er auch Jaques Monod kennen. J. Monod wurde am 9. Februar 1910 in Paris geboren und arbeitete nach seiner Promotion an der Universität Paris ebenfalls am Institut Pasteur. Für ihre Entdeckungen wurden alle drei 1965 mit dem Nobelpreis für Physiologie/Medizin geehrt.
Um nun ihre Hypothese, ihre Experimente und das daraus folgende Modell zu verstehen, gehen wir einen Schritt zurück zum Beispiel der enzymatischen Adaptation von E. coli Bakterien an Glucose/Lactose. Zu jener Zeit waren drei Mutanten-Stämme von E. coli bekannt, welche einen Einfluss auf die enzymatische Adaptation an Glucose/Lactose hatten. Als Mutanten werden hier Stämme bezeichnet, welche minimale Änderungen in ihrer DNA aufweisen. Die drei Mutanten werden als z– Stamm, y– Stamm und i– Stamm bezeichnet und haben folgende Eigenschaften:
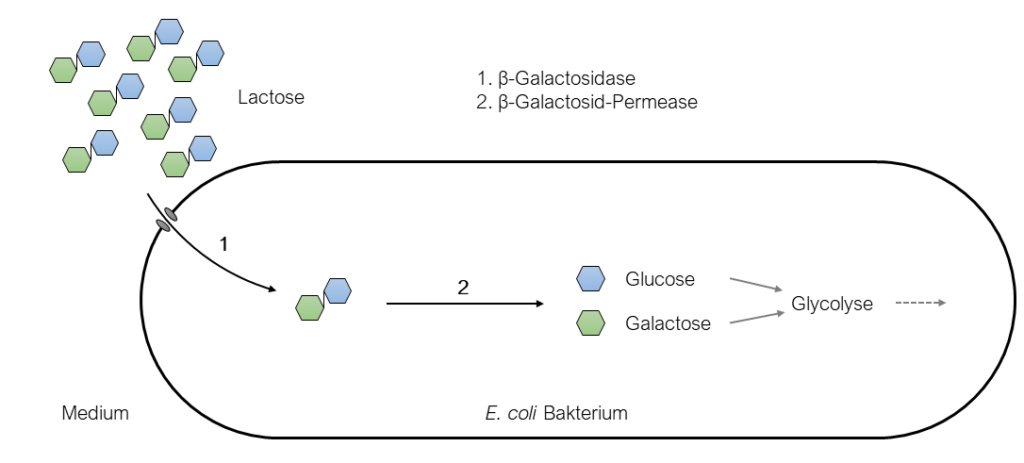
z– Stamm: kann das Protein β-Galactosidase nicht bilden. Bei diesem Protein handelt es sich um ein Enzym, welches die Spaltung der Lactose in Galactose und Glucose sowie die Umwandlung von Lactose in Allolactose katalysiert und somit den Beginn des Lactose-Abbaus bildet.
y– Stamm: kann das Protein β-Galactosid-Permease nicht bilden. Bei der Permease handelt es sich um ein Protein, welches die im Medium befindliche Lactose, in das innere des Bakteriums transportiert.
i– Stamm: kann sowohl β-Galactosidase als auch β-Galactosid-Permease Abwesenheit des Inducers bilden
Schaut man sich im Genom von E. coli an, in welcher Region diese Mutationen liegen, fällt einem auf, dass die alle in einem Bereich vorkommen, welcher von WissenschaftlerInnen als Lac-Bereich bezeichnet wird. Der Grund für diese Bezeichnung ist, dass diese Region die genetischen Informationen zur Bildung der Enzyme enthält, welche Lactose aus dem Medium ins Zellinnere transportieren und abbauen (β-Galactosidase, Galactosidase-Permease, β-Galactosid-Transacetylase)
Aufgrund ihrer Lage auf dem Genom und den Folgen der jeweiligen Mutation, gingen F. Jacob und J. Monod davon aus, dass die z– Mutation auf dem Gen für die β-Galactosidase und die y– Mutation auf dem Gen für die β-Galactosid-Permease liegen muss. Anders hingegen sieht es für die i– Mutation aus. Diese konnte zunächst nicht erklärt werden, da sie die Expression mehrerer Gene beeinflusst und die Mutation an einer gänzlich anderen Stelle im Genom aufkommt als die z– und die i– Mutation. Das bedeutet wiederum, dass die i– Mutation nicht das Gen für die Galactosidase und Permease direkt trifft, sondern die Regulierung dieser beeinflusst. Um diesem Phänomen auf den Grund zu kommen, komplementierten sie ein i– Bakterium mit der DNA der Region i (i+). Das so entstandene neue Bakterium hat immer noch die i– Mutation in seinem Genom, besitzt jetzt aber zusätzlich ein kleines DNA-Molekül, welches die nicht mutierte DNA der i Region beinhaltet. Wir nennen den neu entstandenen Stamm i–i+ (da er sowohl die i– als auch die i+ DNA enthält). Untersuchungen des neuen Stamms ergaben, dass durch Komplementation das Enzym β-Galactosidase und das Protein β-Galactosid-Permease erneut nur in Anwesenheit des Inducers (Lactose) synthetisiert werden. Die i–i+ Bakterien verhalten sich also wieder wie die nicht mutierten Bakterien, was wiederum bedeutet, dass die integrierte i+ Region dominant bezüglich der Genregulation gegenüber der mutierten i– Region ist. F. Jacob und J. Monod schlussfolgerten daraus, dass die Region i die Information zur Bildung eines bestimmten Proteins beinhalten muss, die die Expression von der β-Galactosidase und das Protein β-Galactosid-Permease reguliert. E. coli Bakterien, welche keine Mutation in der Region i ihres Genoms haben, bilden demnach dieses Protein, welches daraufhin dafür sorgt, dass β-Galactosidase und β-Galactosid-Permease nur in Anwesenheit von Lactose gebildet werden. Hat das Bakterium nun die mutierte i– Region in seinem Genom, kann dieses Protein nicht gebildet werden und β-Galactosidase und β-Galactosid-Permease werden dauerhaft gebildet. Bringt man jedoch die natürliche i Region in das mutierte Bakterium ein, (i–i+) kann das Protein erneut gebildet werden und die Expression der β-Galactosidase und β-Galactosid-Permease findet wieder nur in Anwesenheit von Lactose statt.
Eine Frage, die sich die WissenschaftlerInnen diesbezüglich lange stellten, war, ob es sich bei diesem regulierenden Protein um einen Aktivator (ein Protein, dass unter bestimmten Umständen die Expression der β-Galactosidase und der β-Galactosid-Permease aktiviert) oder um einen Repressor (ein Protein, dass die Expression der β-Galactosidase und der β-Galactosid-Permease verhindert und nur unter bestimmten Bedingungen ermöglicht) handelt.
Der Physiker und Molekularbiologe Leo Szilizard postulierte seinerzeit bei einem Gespräch mit J. Monod, dass es sich nur um eine negative Regulation handeln könnte, weil diese schlichtweg einfacher für das Bakterium umzusetzen sei. Er meinte, dass der Aufwand geringer sei, den Start einer Reaktion zu verhindern als diese zu induzieren. Auf das Modell der Lactose-Abbau-Regulation bezogen würde das bedeuten, dass die Anwesenheit von dem regulierenden Protein (wie in einem i+ Bakterium) dafür sorgt, dass keine β-Galactosidase und β-Galactosid-Permease gebildet werden. In Abwesenheit des Proteins (wie in einem i– Bakterium) würde deren Expression nicht verhindert und beide Proteine werden gebildet. Die Antwort auf die Frage, ob es sich bei diesem Protein nun tatsächlich um einen Repressor handelt, lieferte erneut der Komplementations-Versuch von Jacob und Monod. Dadurch dass in dem i-i+ Bakterium erneut nur β-Galactosidase und β-Galactosid-Permease in Anwesenheit von Lactose gebildet werden können, spricht das für die Theorie von L. Szilizard, dass das in den Bakterien erneut anwesende regulierende Protein gebildet wird und die Expression von β-Galactosidase und β-Galactosid-Permease nur in Anwesenheit von Lactose auftritt. Der Lactose wird dabei eine besondere Rolle zuteil: es kann nun geschlussfolgert werden, dass sie die Rolle als „Inducer“ dahin ausübt, indem sie das Repressor-Protein in seiner Funktion hindert. Des Weiteren postulieren Jacob und Monod, dass der Repressor nur funktionieren könnte, wenn er an eine bestimmte Region der RNA binden würde, welche es verhindert, dass die beiden Proteine gebildet werden. Diese Theorie würde einige Observationen bei Bakterien Mutanten erklären, welche keine Mutation in der Region I (Repressor), Z (β-Galactosidase) oder Y (β-Galactosid-Permease) aufwiesen, jedoch trotzdem konstitutiv β-Galactosidase und β-Galactosid-Permease bilden. Kartierungen ergaben, dass diese Bakterien Mutationen in dem Bereich vor Z und Y aufweisen. Jacob und Monod diesem Bereich, von welchem Sie ausgingen, dass der Repressor diesen bindet, den Namen „Operator“ (O) (Jacob & Monod 1959)
Neben der Regulation des Lactoseabbaus, gab es zu jeder Zeit weitere Systeme an deren Regulation geforscht wurde. Zu den bekanntesten gehörten:
1. Regulation der Synthese von DNA-Reparaturenzymen bei hoher UV Belastung in der Bakteriophage Phage λ (Jacob, 1954)
2. Bakterielle Regulation der Synthese der Aminosäure Tryptophan (Cohen-Bazire & Monod, 1953)
3. Bakterielle Regulation der Synthese der Aminosäure Arginine (Gorini & Maas, 1957)
4. Bakterielle Regulation der Synthese der Aminosäure Methionin (Cohn et al., 1953)
F. Jacob hatte schließlich die brillante Idee, die bekannten bakteriellen Systeme der Expressions-Regulation mit dem der Lactose zu vergleichen (Jacob, 1988). Dabei erkannte er einige Gemeinsamkeiten! Gemeinsam mit L. Monod fügte er alle zu der Zeit bekannten Entdeckungen zu einem Modell zusammen, welches zum ersten Mal in der Geschichte die Regulation der bakteriellen Genexpression zusammenfasst. Sie gaben dem Modell den Namen: „Operon-Model“, umgangssprachlich wird es häufig auch Jacob-Monod-Modell genannt (Paradee et al., 1959).
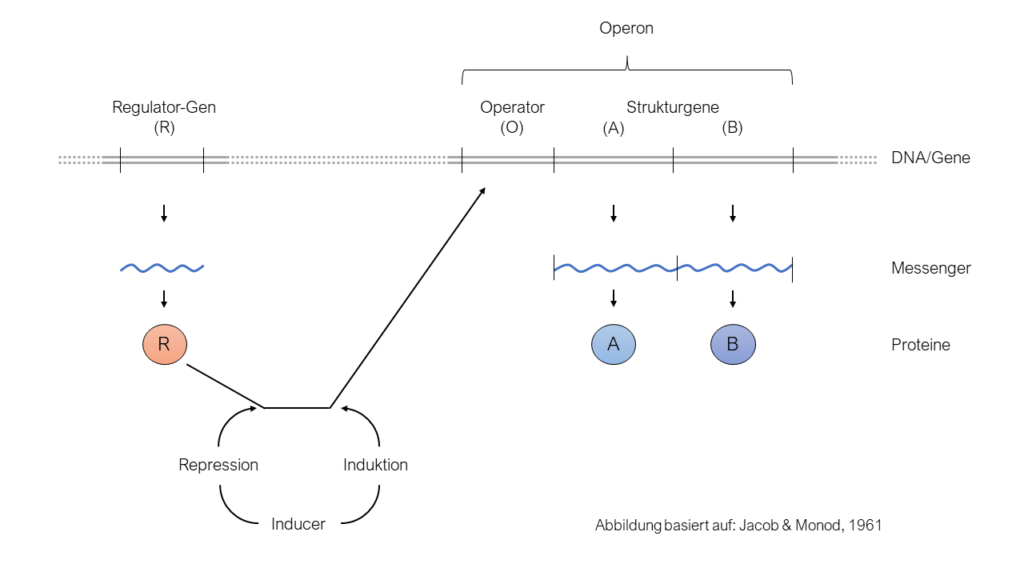
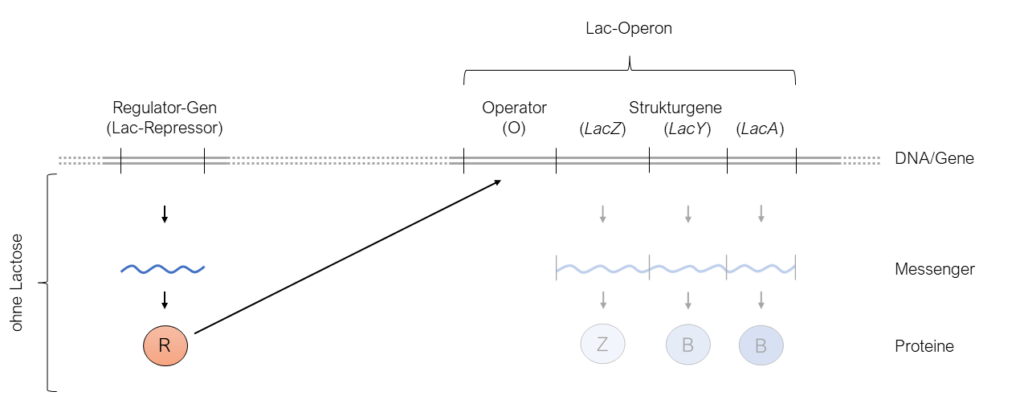
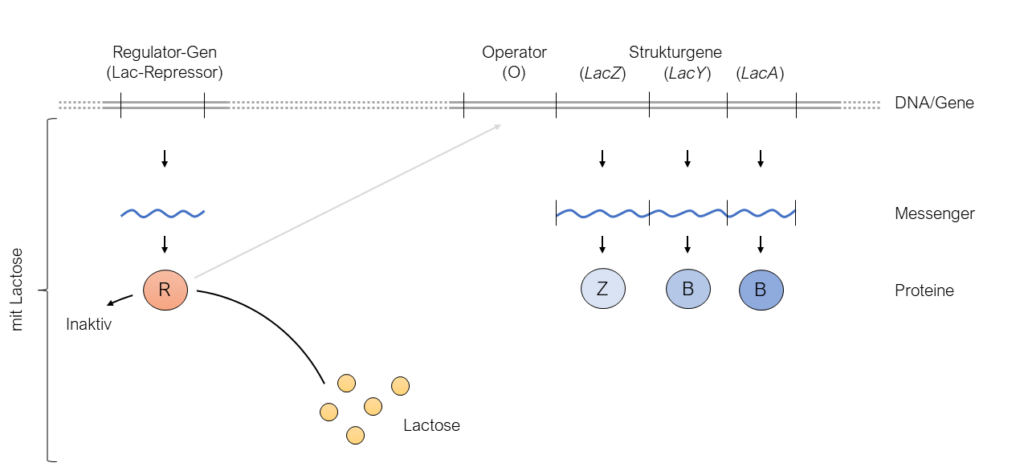
Nach dem Jacob-Monod-Modell kann die bakterielle DNA in verschiedene Bereiche unterteilt werden, so gibt es Gene, welche für Proteine kodieren, aber auch Bereiche, welche Regulatorische Zwecke dienen (siehe den bereits eingeführten „Operator“). Gene, welche für Proteine kodieren, die in Ihrer Funktion voneinander abhängig bzw. aufeinander angewiesen sind, liegen sehr nahe beieinander. Dies ermöglicht es dem Bakterium alle diese Gene gleichzeitig zu regulieren und so enorme Mengen an Energie gegenüber dem Fall einzusparen, wenn die Expression jedes Genes allein reguliert werden. Der DNA-Abschnitt, welcher den Operator sowie die zu regulierende Gene beinhaltet, wird unter dem Begriff „Operon“ zusammengefasst, der auch namensgebend für das Modell war (siehe oben). An anderer Stelle des Genoms befindet sich ein Gen, das für einen Protein kodiert, welches die Expression der Gene reguliert, die sich in einem Operon befinden. Das Protein wird dabei, je nachdem, ob es sich um einen Aktivator oder um einen Repressor handelt, durch die Anwesenheit eines Inducers aktiviert oder deaktiviert. Zu erwähnen ist zudem, dass jedes Regulierendes Protein, die Expression bestimmter Gene kontrolliert. Am vorherigen Beispiel der Lactose würde das bedeuten, dass der in diesem Zusammenhang entdeckte Regulator, welcher als Repressor identifiziert wurde und von nun an Lac-Repressor genannt wird (Lac steht für Lactose), spezifisch mit der Operator-Sequenz interagiert, welche die Expression der β-Galactosidase (LacZ) und β-Galactosid-Permease (LacY) reguliert. Später erkannten WissenschaftlerInnen, dass noch ein weiteres Gen zu dem Lac-Operon gehört: LacA. Dieses kodiert für das Protein β-Galactosid-Transacetylase. Der DNA-Abschnitt, welcher diesen Operator sowie die Gene für die β-Galactosidase (LacZ), β-Galactosid-Permease (LacY) und β-Galactosid-Transacetylase beinhaltet, wird Lac-Operon genannt. Nach Jacob & Monod, interagiert der Lac-Repressor mit der Operator-Sequenz in Abwesenheit der Lactose und verhindert so die Expression der dahinter folgenden Gene. In Anwesenheit der Lactose hingegen wird der Lac-Repressor in seiner Funktion inaktiviert und erlaubt es so, die Expression der darauffolgenden Gene.
Mit ihrer Forschung im Bereich der Regulation der Genexpression und ihren Entdeckungen, welche auf das Zusammentragen aller bekannten Informationen zu diesem Gebiet von allen darin beteiligten AkteurInnen beruhen, ebneten F. Jacob und L. Monod ganz neue Wege für die Molekularbiologie. Sie präsentierten als erste Forscher ein fundiertes Modell, wie die Expression von Genen in Bakterien durch äußere Faktoren beeinflusst und reguliert werden kann. Ihre Forschung wurde von vielen Arbeitsgruppen weltweit aufgegriffen, die weitere Details im Lac-Operon erforschten oder untersuchen wollten, ob und wie die Expression in tierischen und pflanzlichen Zellen reguliert wird.
Autor: SV
Literatur
Crick FHC (1964) On the Genetic Code. Nobel Lectures physiology or medizing.
Cohen-Bazire G, MonodJ (1953) L´effect inhibition spécifique dans la biosynthése de la tryptophanedesmase by Aerobacter aerogens. C R Hebd Seances Acad Sci. 236: 530-532.
Cohn M, Cohen GN, Monod J (1953) L’effect inhibiteur spécifique de la méthionine dans la formation de la méthionine-synthetase chez Escherichia coli. C R Hebd Seances Acad Sci. 236: 746-748.
Dienert F (1900) Sur la fermentation du galactose et sur l´accoutumance des lavures á ce sucre. Ann Inst Pasteur. 14: 139-189.
Duclaux E (1898) Traité de microbiologie. Masson et Cie. Paris.
Gamow G (1954) Possible Relation between Deoxyribonucleic Acid and Protein Structures. Nature. 173: 218.
Gorini L, Maas WK (1957) The potential for the formation of a biosynthetic enzyme in Escherichia coli. Biochim Biophys Acta. 25(1): 208-209.
Jacob F (1954) Les bacteries lysogenes et la notion de provirus. Paris. Masson et Cie.
Jacob F (1988) The statue within: an autobiography. New York: Basic Books.
Jacob F, Monod J (1959) Genes of structure and genes of regulation in the biosynthesis of proteins. C R Hebd Seances Acad Sci. 149: 1282-1284.
Jacob F, Monod J (1961) Genetic regulatory mechanisms in the synthesis of proteins. J Mol Biol. 3: 318-356.
Pardee A, Jacob F, Monod J (1959) The genetic control and cytoplasmic expression of “inducibility” in the synthesis of β-galactosidase by E. coli. J Mol Biol. 1: 165-178.
Vogel H (1957) Repression and induction as control mechanisms of enzyme biogenesis: The “adaptive” formation of acetylo-ornithinase. The chemical basis of heredity. John Hopkins Press. 267-289.
Watson JD (1663) Involvement of RNA in the synthesis of proteins. Science. 140(3562): 17-26.
