James Watson und Francis Crick veröffentlichten 1953 ihre Theorie über die molekulare Struktur der DNA, die noch im selben Jahr durch Rosalind Franklin wissenschaftlich bestätigt wurde (siehe 1953 – Die Strukturaufklärung der DNA). Durch ihre Arbeiten wissen wir heute, dass die DNA aus zwei Strängen besteht, die eine sich windende Helix formen. Die Stränge bestehen aus einer sich wiederholenden Verbindung aus Phosphorsäure und Desoxyribose, die das Rückgrat bilden, sowie einer der vier Basen Adenin (A), Thymin (T), Guanin (G) oder Cytosin (C), die jeweils mit einer Desoxyribose verbunden sind. Die ins Innere der Helix ragenden Basen eines Stranges bilden Wasserstoffbrücken zu den komplementären Basen des anderen Stranges und stabilisieren so die Struktur.
Eine entschlüsselte Nukleinsäuresequenz ist der Schlüssel zum Verständnis des Lebens auf molekularer Ebene. Sie verrät, welche Gene den Bauplan für bestimmte Proteine enthalten, wie diese Gene reguliert werden, wo Mutationen auftreten können und wie eng verschiedene Organismen evolutionär miteinander verwandt sind. Doch bevor all diese Fragen beantwortet werden konnten, musste zunächst eine ganz grundlegende Hürde überwunden werden: Wie liest man überhaupt die Reihenfolge der Bausteine von DNA oder RNA?
Der erste entscheidende Schritt zur Sequenzierung von Nukleinsäuren gelang Robert W. Holley. Im Jahr 1965 veröffentlichte er eine Arbeit, in der er erstmals die vollständige Sequenz einer Transfer-RNA (tRNA) mithilfe der Enzyme RNase A und RNase T1 bestimmte. RNasen sind Enzyme, die RNA an bestimmten Stellen spalten. Während RNase T1 nach Guanin (G) schneidet, spaltet RNase A nach Cytosin (C) und Uracil (U). Holley behandelte eine isolierte tRNA mit diesen Enzymen in unterschiedlichen Kombinationen und Inkubationszeiten. So erhielt er eine Art Puzzle aus unterschiedlich großen RNA-Stücken, die er analysierte und zusammensetzte (Holley et al., 1965). Mühevoll gelang ihm so die erste vollständige Sequenzierung einer RNA. Für diese Leistung erhielt er 1986 den Nobelpreis.
Die erste DNA-Sequenzierung wurde 1970 von Ray Wu beschrieben. Er arbeitete mit der DNA des Bakteriophagens λ, die an ihren Enden kurze, einzelsträngige Überhänge besitzt. Mithilfe einer DNA-Polymerase und radioaktiv markierten Bausteinen (dATP, dCTP, dGTP, dTTP) füllte er diese Überhänge wieder zu einem Doppelstrang auf. Die eingebauten radioaktiven Nukleotide machten es möglich, die Anzahl der eingebauten Basen zu bestimmen (Wu, 1970). Ähnlich wie Holley die RNA zerschnitt, spaltete Wu die markierte DNA in kleinere Fragmente und rekonstruierte daraus die Abfolge.
Fünf Jahre später entwickelten Frederick Sanger und Alan Coulson die sogenannte Plus/Minus-Methode. Hierfür wird die DNA zunächst einzelsträngig vorgelegt und mit Hilfe einer DNA-Polymerase der komplementäre Strang synthetisiert. Bei der Minus-Reaktion fehlen jeweils bestimmte Nukleotide, sodass die Synthese an den entsprechenden Stellen stoppt. Bei der Plus-Reaktion ist jeweils nur ein bestimmtes Nukleotid vorhanden. Trägt man die Produkte auf ein Polyacrylamidgel auf, kann man die Sequenz Stück für Stück ablesen. Allerdings war diese Methode sehr aufwendig und für lange DNA-Stücke ungeeignet.
Schon 1977 gelang Sanger ein Durchbruch: die Dideoxy-Methode, besser bekannt als Sanger-Sequenzierung. Hierbei werden den Reaktionsansätzen spezielle Bausteine, die Dideoxynukleotide (ddNTPs), zugegeben. Diese besitzen keine 3’-OH-Gruppe. Sobald sie eingebaut werden, bricht die DNA-Synthese ab. Dadurch entstehen DNA-Fragmente unterschiedlicher Länge, die im Gel sauber getrennt werden können. Die Reihenfolge der Fragmente zeigt die DNA-Sequenz. Diese Methode war viel zuverlässiger und erlaubte erstmals die Sequenzierung langer DNA-Stücke.
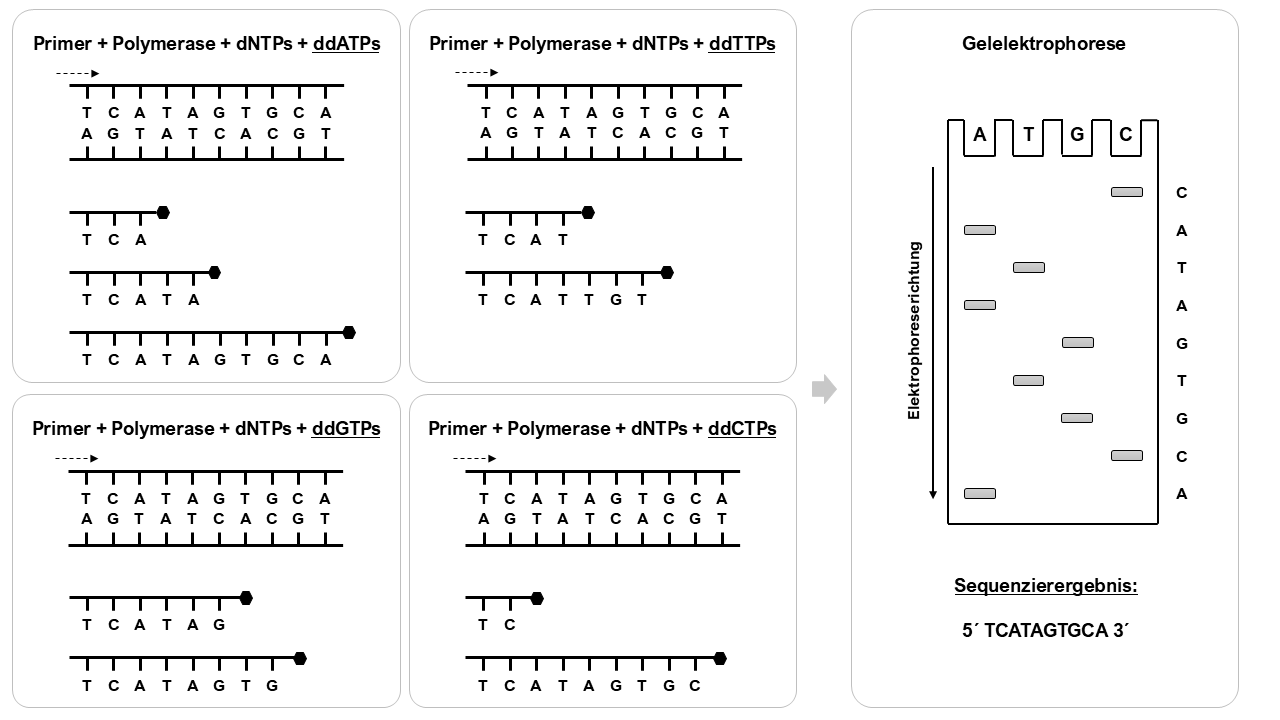
Die Sanger-Sequenzierung bildete die Grundlage für das große Human Genome Project (HGP – Humangenomprojekt), das 1990 startete und 2003 abgeschlossen wurde. Ziel des Projekts war es, das gesamte menschliche Genom zu entschlüsseln. Für seine bahnbrechenden Arbeiten erhielt Frederick Sanger 1980 seinen zweiten Nobelpreis für Chemie. Seinen ersten Nobelpreis hatte er bereits 1958 für die Aufklärung der Struktur des Proteins Insulin erhalten
In den folgenden Jahrzehnten wurde die Methode weiterentwickelt. Besonders wichtig war die Einführung von fluoreszenzmarkierten ddNTPs, wodurch man alle Reaktionen in einem Ansatz kombinieren konnte. Die Fragmente wurden nicht mehr nur im Gel, sondern auch über Kapillarelektrophorese getrennt, wobei ein Laser die Fluorophore anregt und ein Detektor die Farben erkennt. Das Ergebnis: ein buntes Elektropherogramm.
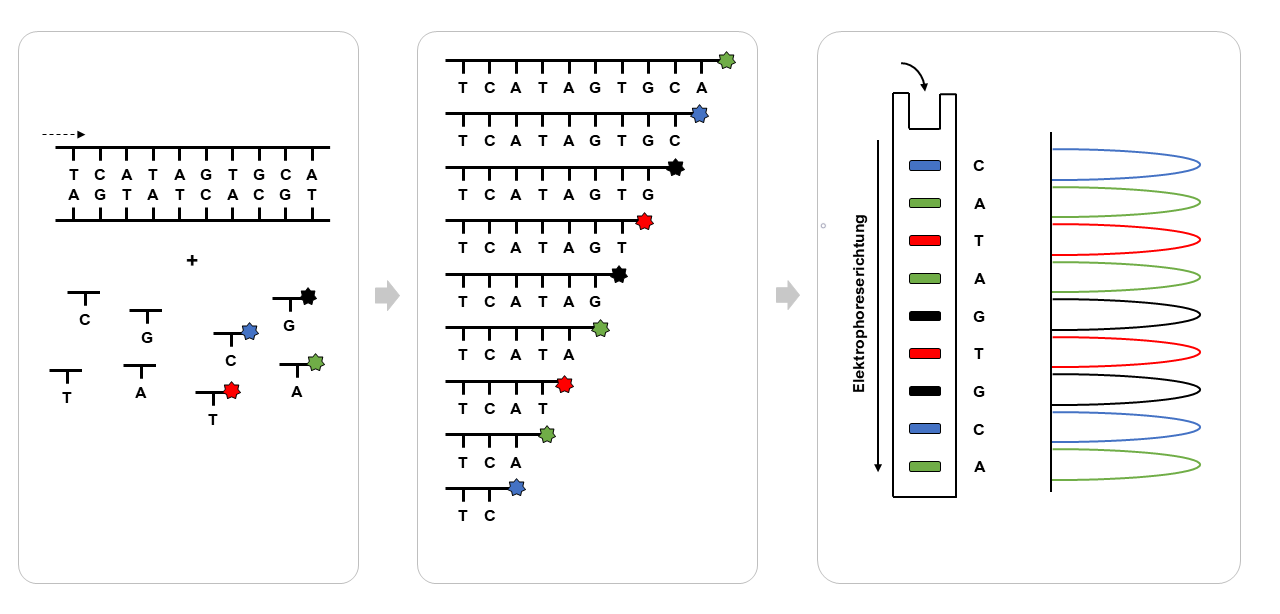
Diese Verfahren werden heute als erste Generation der Sequenzierung bezeichnet. Ab etwa 2005 kamen neue Methoden hinzu, die man als Next Generation Sequencing (NGS) zusammenfasst, etwa die Pyrosequenzierung oder die Illumina-Technologie. Seit einigen Jahren gibt es zusätzlich sogenannte Third Generation Sequencing-Methoden, etwa von Pacific Biosciences oder Oxford Nanopore. Sie ermöglichen noch längere Sequenzierungen in kürzerer Zeit – und oft auch direkt am DNA-Molekül. Auf diese modernen Verfahren gehen wir in einem eigenen Artikel noch genauer ein.
Author: SV
Literatur
Holley RW, Apgar J, Everett GA, et al. (1965) Structure of a ribonucleic acid. Science 147(3664): 1462–1465.
Wu R (1970) Nucleotide sequence analysis of DNA: I. Partial sequence of the cohesive ends of bacteriophage λ and 186 DNA. J Mol Biol 51(3): 501–521.
Sanger F, Coulson AR (1975) A rapid method for determining sequences in DNA by primed synthesis with DNA polymerase. J Mol Biol 94(3): 441–448.
Sanger F, Nicklen S, Coulson AR (1977) DNA sequencing with chain-terminating inhibitors. Proc Natl Acad Sci USA 74(12): 5463–5467.
