Wie in dem vorherigen Artikel „Aspekte der Molekularbiologie – „Die Replikation der DNA“ beschrieben, haben Franklin Stahl und Matthew Meselson herausgefunden, dass sich die DNA semikonservativ repliziert (Messelson & Stahl, 1958). Das bedeutet, dass sich bei diesem Vorgang die doppelsträngige DNA in ihre Einzelstränge teilt und der jeweils komplementäre Strang neu synthetisiert wird. Die nächste zentrale Frage war daher, wie dieser Prozess genau abläuft und ob er sich auch im Labor (in vitro) nachstellen lässt.
Um zu verstehen, wie die Replikation im Detail funktioniert, ist es wichtig zu wissen, welche Moleküle an diesem Prozess beteiligt sind. Eine zentrale Rolle spielt dabei die DNA-Polymerase, ein Protein, das die Synthese eines neuen DNA-Strangs katalysiert. Damit die DNA-Polymerase ihre Arbeit aufnehmen kann, muss sie sich zunächst an die DNA anlagern. Diese Anlagerung ist jedoch nur an doppelsträngigen Bereichen möglich. Deshalb heften sich kurze DNA-Abschnitte, sogenannte Primer, an die einzelsträngige DNA und schaffen so die notwendigen Andockstellen und Startpunkte für die Polymerase. Im lebenden Organismus (in vivo) übernehmen kurze RNA-Moleküle diese Funktion, indem sie zusammen mit der DNA einen kurzen Doppelstrang bilden, an den sich die Polymerase binden kann.
In den 70er-Jahren hat der norwegische Forscher Kjell Kleppe im Labor von Har Gobind Khorana an der University of Wisconsin gearbeitet. Während seiner Forschungszeit untersuchte er grundlegende Eigenschaften von Primern (Kleppe et al., 1971). Die erste Frage, die er versuchte zu beantworten, war, wie lange die Nukleotid-Kette eines Primer sinnvollerweise sein sollte. Um das herauszufinden, synthetisierte Kleppe einzelsträngige DNA-Moleküle: ein langes DNA-Molekül, das von einer Polymerase komplementiert werden soll (= Template), sowie kürzere Sequenzen mit unterschiedlicher Länge (4, 5, 7 und 9 Basen), die als Primer fungieren sollten. In einem Reaktionsmix wurde das Template mit einem Primer bestimmter Länge sowie radioaktiv markierten Nukleotiden, einer DNA-Polymerase und einer passenden chemischen Umgebung (eine Puffersubstanz sowie Magnesium-Ionen) kombiniert. Nach einer Reaktionszeit wurde die Radioaktivität des Produktes gemessen. Je radioaktiver es war, desto mehr Nukleotide (radioaktiv markiert) wurden von der DNA-Polymerase zu einem Strang synthetisiert. Die Ergebnisse zeigten, dass nur die Primer aus 7 und 9 Nukleotiden in der Lage waren, als Andockstationen der DNA-Polymerase zu dienen und so die Synthese des komplementären DNA-Strangs zu ermöglichen.
In den folgenden Jahren kam unter Wissenschaftlern die Idee auf, ob man DNA nicht nur replizieren, sondern auch vervielfältigen könnte. Der in der Firma „Cetus Corporation“ forschende Kary B. Mullis brachte 1983 mit seiner Erfindung der PCR (Polymerase Chain Reaction – Polymerase-Kettenreaktion) die entscheidenden Puzzleteile zusammen und war der Erste, der in vitro DNA im Labor vervielfältigen konnte. In seiner Autobiografie beschreibt er, dass er ein begeisterter Surfer war und in den 1960er-Jahren mehrmals LSD konsumiert habe (Mullis, 1998). Die Idee der PCR sei ihm dabei während einer nächtlichen Autofahrt zu seinem Ferienhaus im Norden Kaliforniens gekommen, und fragwürdiger Weise behauptete er, dass er ohne den Einfluss von LSD niemals darauf gekommen wäre.
Doch wie funktioniert nun die PCR nach Kary B. Mullis? Wie bereits einige Wissenschaftler zuvor, kombinierte er in einem Reaktionsgefäß die zu vervielfältigende DNA, zwei Primer, welche den Bereich markieren, der vervielfältigt werden soll, eine DNA-Polymerase, dNTPs sowie einen Puffer, der die nötige chemische Umgebung liefert. Eine typische PCR-Reaktion besteht aus drei Schritten:
1. Denaturierung: Der Reaktionsansatz wird ohne die Polymerase für etwa 30 Sekunden bei 95 °C inkubiert. Das sorgt dafür, dass die doppelsträngige DNA denaturiert und in zwei Einzelsträngen vorliegt.
2. Primer-Hybridisierung (Annealing): Die Temperatur wird nun auf etwa 55–65 °C gesenkt. Das sorgt dafür, dass die Primer sich an die jeweils komplementären Bereiche der DNA anlagern können und durch Watson-Crick-Basenpaarungen stabilisiert werden.
3. Elongation: Nach Zugabe der Polymerase kann diese nun bei etwa 72 °C ihre Aufgabe erfüllen. Sie lagert sich an den durch einen Primer erzeugten doppelsträngigen Bereich an und fängt mit der Synthese des neuen DNA-Strangs an.
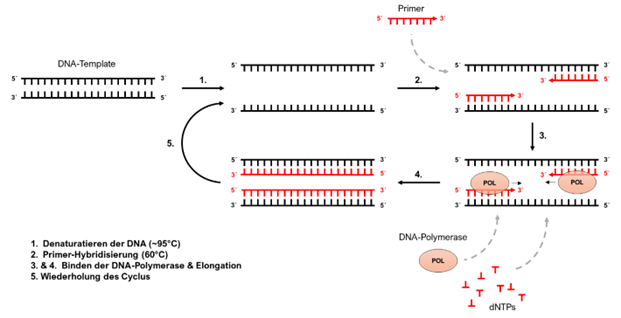
Das Besondere bei Kary B. Mullis: Im Gegensatz zu seinen Vorgängern hat er diese drei Schritte immer wieder wiederholt, sodass es zu einer exponentiellen Anreicherung der zu amplifizierenden DNA-Region kam. Erfolgt das Ganze in einem sogenannten Thermocycler, welcher die Temperaturen automatisch nach Voreinstellung ändert, verläuft der gesamte Vorgang sogar halbwegs automatisch ab. Das war die Geburtsstunde der PCR!
Dem aufmerksamen Leser fällt jedoch eine Sache auf: Es muss bei jeder Wiederholung neue DNA-Polymerase hinzugegeben werden, da diese bei jedem Zyklus aus Denaturierung/Hybridisierung und Elongation ebenfalls denaturiert. Das ist nicht nur arbeitsaufwendig, sondern verbraucht auch Unmengen an Material.
Die Lösung zu diesem Problem wurde im Artenreichtum der Natur gefunden! Man wusste bereits, dass Leben auch unter extremen Bedingungen existieren kann. 1969 entdeckten Forscher der Indiana University im Yellowstone-Nationalpark an einer der heißen Thermalquellen das Bakterium Thermus aquaticus (Brock & Freeze, 1969). Es lebt bei Temperaturen um die 80 °C! Das bedeutet im Gegenzug, dass alle biologischen Prozesse in diesem Bakterium bei solch hohen Temperaturen ebenfalls ablaufen können – so auch die DNA-Replikation. Die DNA-Polymerase des Bakteriums (aufgrund dessen Namens auch Taq-Polymerase genannt) wurde 1976 erstmals von A. Chien, D. B. Edgar und J. M. Trela isoliert (Chien et al., 1976). Ein Team an der Cetus Corporation, bestehend aus R. K. Saiki, D. H. Gelfand, S. Stoffel, S. J. Scharf, R. Higuchi, G. T. Horn, K. B. Mullis und H. A. Erlich, entwickelte die PCR-Methode nun weiter, indem sie die Taq-Polymerase als DNA-Polymerase für den Prozess nach Mullis verwendeten (Saiki et al., 1988). Der Vorteil: Die Zugabe erfolgte einmalig zu Beginn der Reaktion. Da die Taq-Polymerase extreme Hitze aushalten kann, denaturiert sie nicht bei jedem PCR-Zyklus – und der Vorgang kann nun ganz automatisch ablaufen! Im Jahr 1993 erhielt Mullis den Nobelpreis für Chemie für seine Erfindung der PCR-Methode.
Ein Patent der Firma Cetus Corporation über die PCR sowie die Taq-Polymerase wurde 1991 an die Firma Roche verkauft, was zu einer Welle an Klagen, u. a. von der Firma Promega, führte. Trotz einiger Patentrückrufe behielt die Firma Roche alle Rechte an der PCR-Methode. Nach Ablauf der Patente 2005/2006 explodierte die Nutzung der PCR. Aus einem High-Tech-Verfahren wurde eine Standardmethode, die heute in jedem molekularbiologischen Labor Anwendung findet. Sie entwickelte sich mit neuen Puffern und DNA-Polymerasen immer weiter und wird in vielen Bereichen erfolgreich eingesetzt: In der Forschung wird sie für das Klonieren von Genen in Vektoren sowie für die DNA-Sequenzierung verwendet. In der Diagnostik wird sie genutzt, um Erbkrankheiten, Verunreinigungen sowie virale oder bakterielle Infekte zu erkennen (einige erinnern sich noch an die PCR-Tests während der Corona-Pandemie). Aber auch in der Forensik ist sie eine weit verbreitete, jedoch umstrittene Methode.
Autor: SV
Literatur
Meselson M & Stahl FW (1958) The replication of DNA in Escherichia coli. Proc Natl Acad Sci U S A, 44: 671–682.
Kleppe K, Ohtsuka E, Kleppe R, Molineux I & Khorana HG (1971) Studies on polynucleotides. XCVI. Repair replications of short synthetic DNA’s as catalyzed by DNA polymerases. J Mol Biol, 56(2): 341–361.
Mullis K (1998) Dancing naked in the mind field. New York: Pantheon Books.
Brock TD & Freeze H (1969) Thermus aquaticus gen. n. and sp. n., a nonsporulating extreme thermophile. J Bacteriol, 98(1): 289–297.
Chien A, Edgar DB & Trela JM (1976) Deoxyribonucleic acid polymerase from the extreme thermophile Thermus aquaticus. J Bacteriol, 127: 1550–1557.
Saiki RK, Gelfand DH, Stoffel S, Scharf SJ, Higuchi R, Horn GT, Mullis KB & Erlich HA (1988) Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science, 239: 487–491.
